题目内容
13.对某无色溶液进行酸碱性测定,测得结果呈强酸性.下列各组离子中,不可能大量存在的是( )| A. | Mg2+、Ca2+、NO3-、Cl- | B. | Na+、Mg2+、Cl-、SO42- | ||
| C. | K+、Fe3+、Cl-、SO42- | D. | Ba2+、Al3+、Cl-、NO3- |
分析 呈强酸性,含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,则离子能大量共存,并结合离子的颜色来解答.
解答 解:A.该组离子之间不反应,可大量共存,且离子均为无色,故A不选;
B.该组离子之间不反应,可大量共存,且离子均为无色,故B不选;
C.Fe3+为黄色,与溶液无色溶液不符,故C选;
D.该组离子之间不反应,可大量共存,且离子均为无色,故D不选.
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及离子颜色的考查,题目难度不大.

练习册系列答案
相关题目
1.实验室需要配置去100ml 1.0×10-2mol/L的CuSO4溶液,下列玻璃仪器中,一定不要用到的是( )
| A. | 漏斗 | B. | 玻璃棒 | C. | 烧杯 | D. | 容量瓶 |
5.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8g O2的体积为5.6L | |
| B. | 标准状况下,22.4 L H2O所含的分子数为NA | |
| C. | 标准状况下,50mL 0.2mol•L-1的盐酸中含有分子数为0.01NA | |
| D. | 常温常压下,10g氖气含有的原子数为0.5NA个 |
1.一定条件下,H2O2在水溶液中发生分解反应:2H2O2$\frac{\underline{\;一定条件\;}}{\;}$2H2O+O2↑.反应过程中,测得不同时间H2O2的物质的量浓度如下表所示:
(1)在H2O2分解反应中,氧化产物和还原产物的质量之比是8:9.
(2)在0-20min时间内,该反应的平均反应速率v(H2O2)=0.02mol/(L•min).
(3)若反应所用的H2O2溶液为100mL(忽略溶液体积的变化),则80min时,反应共产生O21.44g.
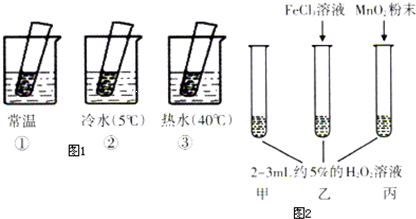
(4)如图1、图2是某学生探究外界条件对H2O2分解反应速率的影响实验装置示意图,请按表格要求填写空白.
实验一:(试管中均为滴有FeCl3溶液的5%H2O2溶液)
实验二:
| t/min | 0 | 20 | 40 | 60 | 80 |
| c(H2O2)/mol•L-1 | 1.0 | 0.60 | 0.40 | 0.20 | 0.10 |
(2)在0-20min时间内,该反应的平均反应速率v(H2O2)=0.02mol/(L•min).
(3)若反应所用的H2O2溶液为100mL(忽略溶液体积的变化),则80min时,反应共产生O21.44g.
(4)如图1、图2是某学生探究外界条件对H2O2分解反应速率的影响实验装置示意图,请按表格要求填写空白.
实验一:(试管中均为滴有FeCl3溶液的5%H2O2溶液)
| 现象 | 结论 | |
| 热水中 | 溶液中有气泡产生,比常温快 | 升高温度,H2O2的分解速率加快 |
| 常温中 | 溶液中有气泡产生,且速度较快 | 无 |
| 冷水中 | 溶液中有气泡产生,比常温慢 | 降低温度,H2O2的分解速率减慢 |
| 现象 | 结论 | |
| 丙加入MnO2 | MnO2能加快化学反应速率 | |
| 乙加入FeCl3 | FeCl3能加快化学反应速率 | |
| 甲不加其他试剂 | 溶液中有少量气泡出现 | 不使用催化剂化学反应速率较小 |
