题目内容
甲~己等元素在周期表中的位置关系如表,甲是形成物质种类最多的元素,庚是原子半径最小的元素,下列判断正确的是( )
| 甲 | 乙 | 丙 | |
| 丁 | 戊 | ||
| 己 |
| A、乙、戊、庚三种元素形成的化合物只含共价键 |
| B、原子半径:甲>乙>丙 |
| C、最高价氧化物对应水化物的酸性:戊>丁>己 |
| D、丁与己的原子序数相差8 |
考点:元素周期律和元素周期表的综合应用
专题:
分析:甲是形成物质种类最多的元素,则甲为C,庚是原子半径最小的元素,则庚为H,由元素在周期表中位置可知,乙为N、丙为O、丁为P、戊为Cl、己为As,结合元素周期律与元素化合物结构解答.
解答:
解:甲是形成物质种类最多的元素,则甲为C,庚是原子半径最小的元素,则庚为H,由元素在周期表中位置可知,乙为N、丙为O、丁为P、戊为Cl、己为As,
A.乙、戊、庚三种元素形成的化合物为NH4Cl,含有离子键、共价键,故A错误;
B.同周期自左而右原子半径进减小,故原子半径:甲>乙>丙,故B正确;
C.同周期自左而右非金属性增强、同主族自上而下非金属性减弱,非金属性越强,最高价含氧酸的酸性越强,故最高价氧化物对应水化物的酸性:戊>丁>己,故C正确;
D.丁与己的原子序数相差18,故D错误,
故选BC.
A.乙、戊、庚三种元素形成的化合物为NH4Cl,含有离子键、共价键,故A错误;
B.同周期自左而右原子半径进减小,故原子半径:甲>乙>丙,故B正确;
C.同周期自左而右非金属性增强、同主族自上而下非金属性减弱,非金属性越强,最高价含氧酸的酸性越强,故最高价氧化物对应水化物的酸性:戊>丁>己,故C正确;
D.丁与己的原子序数相差18,故D错误,
故选BC.
点评:本题考查结构性质位置关系应用,需要熟练掌握元素周期表的结构与元素周期律,难度不大.

练习册系列答案
相关题目
下列关于卤素单质的叙述,正确的是( )
| A、单质的颜色随核电荷数的增加逐渐变浅 |
| B、随核电荷数的增加单质的氧化性逐渐减弱 |
| C、随核电荷数的增加气态氢化物的稳定性逐渐增强 |
| D、单质的熔沸点随核电荷数的增加逐渐降低 |
下列有关实验装置进行的相应实验,不能达到实验目的是( )
A、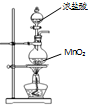 用装置制取氯气 |
B、 用装置除去氯气中的少量氯化氢和水蒸气 |
C、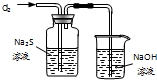 用装置可证明Cl2的氧化性强于S |
D、 用装置可以完成“喷泉”实验 |

 ,请写出其涉及的反应(注明反应的条件
,请写出其涉及的反应(注明反应的条件 A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大.A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族.回答下列问题:
A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大.A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族.回答下列问题: