题目内容
9.空白实验分析是化学实验中常用的一种方法,是指在不加样品的情况下,用与测定样品相同的方法、步骤进行定量分析,把所得结果作为空白值,从样品的分析结果中扣除,这样可以消除由于试剂不纯或试剂干扰等所造成的系统误差.“凯氏定氮法”是经典的测定化合物或混合物中总氮量的一种方法.某化学实验小组成员想通过“凯氏定氮法”实验测定某品牌化肥中的氮含量.实验流程如下:
化肥$→_{加热}^{辅助试剂}$(NH4)2SO4溶液$→_{吹出}^{NaOH}$NH3$→_{吸收}^{H_{3}BO_{3}}$(NH4)2B4O7溶液→用标准盐酸滴定
步骤:①取10.00g化肥样品溶于水,定容至100mL;
②在烧杯中加入10.00mL步骤①中得到的化肥水溶液和辅助试剂,加热使其充分反应;
③反应完毕,将反应液转移到大试管中;
④按如下装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
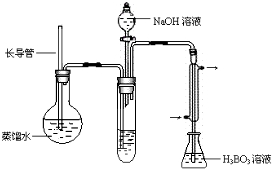
⑤取下锥形瓶,滴加指示剂,用0.2500mol•L-1盐酸标准液滴定;
⑥重复实验操作.
数据记录如下:
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL溶液、0.1g催化剂、20mL浓硫酸 | 33.18 |
| 2 | 10.00mL溶液、0.1g催化剂、20mL浓硫酸 | 33.70 |
| 3 | 10.00mL溶液、0.1g催化剂、20mL浓硫酸 | 33.22 |
| 4 | x |
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl.H3BO3为一元弱酸,在水中发生反应H3BO3+H2O?[B(OH)4]-+H+.pH相同的硼酸溶液、盐酸中,水的电离程度前者大(填“前者大”、“后者大”或“相同”)
(2)步骤③的实验装置中需要加热的仪器是圆底烧瓶(填仪器名称),长导管的作用是防止装置中压力过大而发生危险,防止冷却时发生倒吸.
(3)编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.1g催化剂、20mL浓硫酸,理由是空白、等量对照以消除其他试剂、实验操作等因素引起的误差.
(4)通过计算可得该化肥中的氮含量为116.2-3.5x克/每千克化肥(用含x的代数式表示,要求化简).
分析 (1)滴加盐酸(NH4)2B4O7转化为H3BO3,硼的化合价未变化,发生类似复分解反应,还有氯化铵生成;
(2)用水蒸气将NH3吹出,所以加热圆底烧瓶产生水蒸气,进入试管中将生成的氨气吹出;加热产生水蒸气,装置内压强增加,防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用;
(3)依据编号1、2、3分析可知编号为4的实验应加入的样品和辅助试剂,实验组与对照组的无关变量的影响是相等的,这样通过空白对照实验,对比实验的结果,排除无关变量的影响,则可认定为是来自实验变量的效果,使实验结果更有说服力;
(4)根据N元素守恒,及滴定反应找出N原子与HCl的关系式,根据关系式计算,注意盐酸的体积取3次滴定的平均值减去xml(不含奶时消耗盐酸的体积为xml).
解答 解:(1)硼的化合价未变化,发生类似复分解反应,反应方程式为(NH4)2B4O7+2HCl+5H2O=4 H3BO3+2NH4Cl,H3BO3为一元弱酸,在水中发生反应H3BO3+H2O?[B(OH)4]-+H+.pH相同的硼酸溶液、盐酸中,硼酸电离过程可知,硼酸结合水电离出的氢氧根离子,水电离出氢离子,水的电离程度前者大,
故答案为:(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl;前者大;
(2)加热圆底烧瓶产生水蒸气,进入试管中将生成的氨气吹出;加热产生水蒸气,装置内压强增加,长导管防止装置中压力过大而发生危险,冷却时防止发生倒吸,起安全管作用,
故答案为:圆底烧瓶;防止装置中压力过大而发生危险,防止冷却时发生倒吸;
(3)依据编号1、2、3分析可知编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.1g催化剂、20mL浓硫酸,空白、等量对照使用目的是消除其他试剂、实验操作等因素引起的误差,
故答案为:10.00mL蒸馏水、0.1g催化剂、20mL浓硫酸;空白、等量对照以消除其他试剂、实验操作等因素引起的误差;
(4)盐酸的体积为$\frac{33.18+33.70+33.22}{3}$-xml=(33.34-x)×10-3L,
令10ml该液态奶的含氮量的质量为mg,则
2N~(NH4)2B4O7~2HCl
28g 2mol
mg 0.2500mol•L-1×(33.34-x)×10-3L
所以m=3.5(33.34-x)×10-3g,
100ml中即10.0g含氮量3.5(33.34-x)×10-3g×$\frac{100}{10}$=35(33.34-x)×10-3g
该液态奶的含氮量为氮量的质量=35(33.34-x)×10-3×$\frac{1000}{10}$g/Kg=116.2-3.5x,
故答案为:116.2-3.5x.
点评 本题知识涉及元素化合物、实验原理、化学计算、化学仪器的使用等,侧重考查学生对实验方案理解、元素化合物的知识,难度较大,易错点为计算液态奶的含氮量时盐酸体积应为3次滴定的平均值减去xml(不含奶时消耗盐酸的体积为xml).

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案| A. | M的气态氢化物与其最高价氧化物的水化物之间能相互反应 | |
| B. | N单质能将K从其钠盐的水溶液中置换出来 | |
| C. | N的氢化物沸点高于其它同族元素氢化物的沸点 | |
| D. | P、Q、K对应的最高价氧化物的水化物相互之间可能发生反应 |
 金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:
金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:(1)Ti的基态原子价电子排布式为3d24s2.
(2)纳米TiO2常用作下述反应的催化剂.
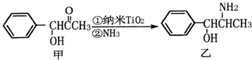
化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C.
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型是共价键、配位键,1mol该配合物中含有的σ键数目是18NA.
(4)通过X-射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
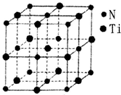
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有12个:Ti原子的配位数为6;此配位原子构成的空间构型为正八面体;该晶胞中N、Ti原子之间的最近距离为a nm.则该氮化钛晶体的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-7})^{3}}$g•cm-3、NA为阿伏加德罗常数的值,只列计算式).
(1)将滤纸用3.5%的NaCl溶液润湿,涂上铁粉、碳粉的混合物,贴在表面皿上.在滤纸上加几滴检验试剂,再缓慢加入NaCl溶液至没过滤纸,操作如图1所示:
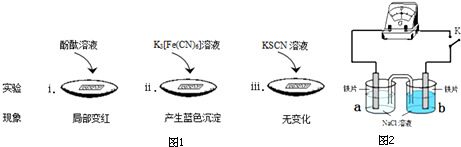
①实验ⅰ的现象说明,得电子的物质是O2.
②碳粉的作用是与铁组成原电池,作原电池的正极.
③为了说明NaCl的作用,需要补充的对照实验是用水代替NaCl溶液进行上述实验.
(2)向图示装置的烧杯a、b中各加入30mL 3.5%的NaCl溶液,闭合K,指针未发生偏转.加热烧杯a,指针向右偏转.
①取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化,b中铁片作正极.
②加热后,指针发生偏转的原因可能是温度升高,Fe还原性增强,反应速率加快.
(3)用图2示装置探究不同浓度NaCl溶液对钢铁腐蚀的影响,向烧杯a、b中各加入30mL不同质量分数的NaCl溶液,实验记录如表所示.
| 实验 | a | b | 指针偏转方向 |
| Ⅰ | 0.1% | 0.01% | 向右 |
| Ⅱ | 0.1% | 3.5% | 向左 |
| Ⅲ | 3.5% | 饱和溶液 | 向右 |
②Ⅲ中,铁在饱和NaCl溶液中不易被腐蚀.
查阅资料可知:在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀.设计实验证明:另取两个烧杯,分别往其中加入铁片和一定量的饱和NaCl溶液,再分别滴加几滴
K3Fe(CN)6溶液,然后往其中一个烧杯中通入O2,观察现象.
(4)根据上述实验,对钢铁腐蚀有影响的因素是温度、NaCl溶液的浓度、O2的浓度.
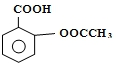 阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途.下列有关说法正确的是( )
阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途.下列有关说法正确的是( )| A. | 与乙酰水杨酸具有相同官能团的芳香族同分异构体共有8种(不考虑立体异构) | |
| B. | 乙酰水杨酸能发生取代、加成、氧化、还原反应 | |
| C. | 乙酰水杨酸的所有原子均在同一平面上 | |
| D. | 服用阿司匹林药量过大时,可出现精神错乱、惊厥甚至昏迷等水杨酸反应,可用硼酸溶液解毒 |

| A. | HR为强酸 | |
| B. | a、b两点所示溶液中水的电离程度相同 | |
| C. | b点溶液中c( NH4+)>c( R-)、c(OH-)>c(H+) | |
| D. | a~c任意点溶液均有c(H+)×c(OH-)=Kw=l.0×l0-14 |
| A. | 241 | B. | 146 | C. | 95 | D. | 336 |
| A. | X、Y、Z的热稳定性逐渐增强 | |
| B. | A、B、C、D只能形成5种单质 | |
| C. | A、B的氧化物的水化物的酸性逐渐增强 | |
| D. | 由B、C、D三种元素组成的化合物中只能形成共价键 |
 Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.
Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.