题目内容
12.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次通过盛有下列哪一组试剂的洗气瓶( )| A. | 澄清石灰水、浓H2SO4 | B. | 酸性KMnO4溶液、浓H2SO4 | ||
| C. | 溴水、浓H2SO4 | D. | 浓H2SO4、NaOH溶液 |
分析 因乙烯与溴水反应,而甲烷不能,除去乙烯得到纯净的甲烷,则利用溴水、洗气可除杂,以此来解答.
解答 解:A.乙烯、甲烷均不与石灰水、浓硫酸反应,不能除杂,故A不选;
B.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,故B不选;
C.乙烯与溴水反应,而甲烷不能,选择溴水、洗气,再利用浓硫酸干燥可除杂,故C选;
D.乙烯、甲烷均不与浓硫酸、NaOH溶液反应,不能除杂,故D不选;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握有机物的结构与性质、性质差异、混合物分离方法选择为解答的关键,侧重分析与应用能力的考查,注意除杂的原则,题目难度不大.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
11.下列说法正确的是( )
| A. | 煤、天然气和石油是纯净物 | |
| B. | 利用化石燃料燃烧放出的热量使分解产生氢气,是氢能开发的研究方向 | |
| C. | 化学电源放电、植物光合作用都能发生化学变化,并伴随能量的转化 | |
| D. | 若化学过程中断开化学键吸收的能量大于形成化学键所放出的能量,则反应放热 |
12.下列条件变化会使H2O的电离平衡向电离方向移动,且pH<7的是( )
| A. | 常温下,向水中加少量稀盐酸 | B. | 将纯水加热到100℃ | ||
| C. | 常温下,向水中加少量Na | D. | 常温下,向水中加少量Na2CO3固体 |
7.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃,1.01×105Pa,64g SO2中含有的原子数为3NA | |
| B. | 足量Fe与1 mol Cl2反应,转移了3NA个电子 | |
| C. | 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
17.常温下,一定量的乙酸溶液与氢氧化钠溶液发生中和反应,下列说法正确的( )
| A. | c(CH3COO-)=c(Na+)时,参加反应的乙酸与氢氧化钠的物质的量之比为1:1 | |
| B. | c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,不一定是醋酸过量 | |
| C. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,一定是氢氧化钠过量 | |
| D. | c(CH3COO-)=c(Na+)时,该溶液一定呈中性 |
4.部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法不正确的是( )


| A. | 简单离子半径的大小顺序g>h>e>f | |
| B. | 与x 形成化合物的沸点:d>z>y | |
| C. | zh3中各原子均满足8电子结构 | |
| D. | x、y、z、d四种元素各自最高价和最低价代数和分别为0、0、2、4 |
1.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数为3.75NA | |
| D. | 235g核素$\stackrel{239}{92}$U发生裂变反应:$\stackrel{239}{92}$ U+$\stackrel{1}{0}$n$\stackrel{裂变}{→}$$\stackrel{90}{38}$Sr+$\stackrel{136}{54}$U+10$\stackrel{1}{0}$n,净产生的中子($\stackrel{1}{0}$n)数为10 NA |
2.N2H4和N2O4反应生成H2O和N2.若反应消耗1mol N2H4,则下列说法正确的是( )
| A. | 产生33.6L N2 | B. | 被还原的N原子为2mol | ||
| C. | 转移电子为4 mol | D. | 还原产物比氧化产物多0.5mol |
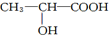 ,
, +2Na→
+2Na→ +H2↑
+H2↑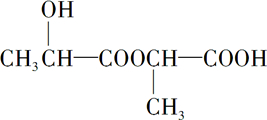 .
.