题目内容
15.实验室有一瓶溶液,标签上标有“BaCl2 0.2mol•L-1”的字样,下面是某同学对该溶液的叙述,正确的是( )| A. | 配制500mL该溶液,可将0.1 mol BaCl2溶于500mL水中 | |
| B. | Ba2+和Cl-的物质的量浓度都是0.1 mol•L-1 | |
| C. | 将该瓶溶液稀释一倍,则所得溶液的c(Cl-)为0.2 mol•L-1 | |
| D. | 从试剂瓶中取该溶液的一半,则所取溶液的物质的量浓度为0.1 mol•L-1 |
分析 A.溶于500mL水为溶剂的体积;
B.由BaCl2 0.2mol•L-1及物质构成计算;
C.稀释前后离子的物质的量不变;
D.溶液具有均一性.
解答 解:A.溶于500mL水为溶剂的体积,应为0.1 mol BaCl2溶于水配制500mL溶液,其浓度为0.2mol•L-1,故A错误;
B.由BaCl2 0.2mol•L-1及物质构成可知,Ba2+和Cl-的物质的量浓度分别为0.2 mol•L-1、0.4 mol•L-1,故B错误;
C.Cl-的物质的量浓度为0.4mol/L,稀释前后离子的物质的量不变,则将该瓶溶液稀释一倍,则所得溶液的c(Cl-)为$\frac{V×0.4mol/L}{2V}$=0.2 mol•L-1,故C正确;
D.溶液具有均一性,则从试剂瓶中取该溶液的一半,则所取溶液的物质的量浓度为0.2 mol•L-1,故D错误;
故选C.
点评 本题考查物质的量浓度的计算,为高频考点,把握物质的量与浓度的关系、溶液的性质为解答的关键,侧重分析与计算能力的考查,注意物质的构成,题目难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
18.下列有关说法不正确的是( )
| A. | 红热的铜丝可以和乙醇发生置换反应产生氢气 | |
| B. | 苯和乙烯都能使溴水褪色,但原理不同 | |
| C. | 淀粉和乙酸乙酯在一定条件下都能发生水解反应 | |
| D. | 乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
6.下列物质的物质的量最大的是( )
| A. | 分子数为 3.01×1023个的SO2 | B. | 0.48 molH2SO4 | ||
| C. | 标准状况下8.96L CH4 | D. | 9g 氖气 |
10.下列关于浓硫酸的叙述正确的是( )
| A. | 浓硫酸具有脱水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体 | |
| D. | 因为浓硫酸在常温下不可与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸 |
7.下列各组物质中,所含分子数相同的是( )
| A. | 10g H2和10g O2 | B. | 11.2L(标准状况)H2O和0.5mol Br2 | ||
| C. | 5.6L N2(标准状况)和11g CO2 | D. | 224mL H2(标准状况)和0.1mol N2 |
4.向含有下列4种离子的溶液中加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
| A. | NO3- | B. | Ba2+ | C. | OH- | D. | Cu2+ |
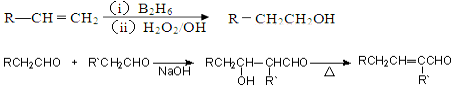
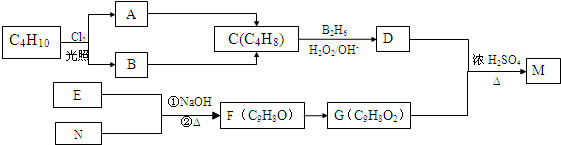
 、
、 ;
; $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$