题目内容
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示.

(1)装置Ⅰ,Ⅱ中能够达到实验目的是(填装置序号) .原理是:
(2)与实验Ⅲ相比,实验Ⅳ的优点是(填选项序号) .
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式) .
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应.
①当石灰水过量时,其离子方程式为 ;
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,所得溶液中溶质的化学式为 ,
(5)装置Ⅲ的气密性如何检查 .

(1)装置Ⅰ,Ⅱ中能够达到实验目的是(填装置序号)
(2)与实验Ⅲ相比,实验Ⅳ的优点是(填选项序号)
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式)
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应.
①当石灰水过量时,其离子方程式为
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,所得溶液中溶质的化学式为
(5)装置Ⅲ的气密性如何检查
考点:探究碳酸钠与碳酸氢钠的性质
专题:实验题
分析:(1)碳酸钠和盐酸反应分两步进行,盐酸和碳酸钠、碳酸氢钠反应都生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊;
(2)根据两个实验装置的特点及区别进行分析;
(3)不直接加热碳酸氢钠就能分解更说明碳酸氢钠不稳定;
(4)①碳酸氢钠和氢氧化钙发生复分解反应;
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,碳酸氢钠和氢氧化钙反应生成碳酸钠、碳酸钙和水;
(5)将导气管末端插入水中,用手握住或利用热毛巾捂容器对该仪器装置微热,观察导管末端是否有气泡逸出,松开手后观察导管末端是否形成一段水柱,检查判断气密性情况.
(2)根据两个实验装置的特点及区别进行分析;
(3)不直接加热碳酸氢钠就能分解更说明碳酸氢钠不稳定;
(4)①碳酸氢钠和氢氧化钙发生复分解反应;
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,碳酸氢钠和氢氧化钙反应生成碳酸钠、碳酸钙和水;
(5)将导气管末端插入水中,用手握住或利用热毛巾捂容器对该仪器装置微热,观察导管末端是否有气泡逸出,松开手后观察导管末端是否形成一段水柱,检查判断气密性情况.
解答:
解:(1)无论碳酸钠还是碳酸氢钠都能和盐酸反应生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊,故Ⅰ无法鉴别;
实验Ⅱ中,盐酸和碳酸氢钠反应立即产生气泡,盐酸和碳酸钠先反应生成碳酸氢钠,碳酸氢钠和盐酸反应生成二氧化碳气体,所以看到的现象不同,故能鉴别碳酸钠和碳酸氢钠,
故答案为:Ⅱ;碳酸氢钠与盐酸反应产生的二氧化碳速率快;
(2)实验Ⅲ、Ⅳ相比,IV可以做到一套装置同时进行两个对比实验,而III不能,故选D,
故答案为:D;
(3)碳酸钠直接加热,碳酸氢钠不直接加热,不直接加热的碳酸氢钠能分解而直接加热的碳酸钠不分解更能说明碳酸氢钠不稳定,
故答案为:NaHCO3;
(4)①当石灰水过量时,离子方程式按照碳酸氢钠的组成书写,反应的离子方程式为:HCO3-+OH-+Ca2+═CaCO3↓+H2O,
故答案为:HCO3-+OH-+Ca2+═CaCO3↓+H2O;
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,反应方程式为:2HCO3-+2OH-+Ca2+═CaCO3↓+H2O+CO32-,所以溶液中的溶质是Na2CO3,
故答案为:Na2CO3;
(5)检查各装置气密性的方法为:将导气管末端插入水中,然后用手握住或利用热毛巾捂容器对该仪器装置微热,观察导管末端有气泡逸出,且松开手后,观察到导管末端形成一段水柱,说明气密性好,
故答案为:将导气管末端插入水中,然后用手握住或利用热毛巾捂容器对该仪器装置微热,导管末端有气泡逸出,且松开手后,观察到导管末端形成一段水柱,说明气密性好.
实验Ⅱ中,盐酸和碳酸氢钠反应立即产生气泡,盐酸和碳酸钠先反应生成碳酸氢钠,碳酸氢钠和盐酸反应生成二氧化碳气体,所以看到的现象不同,故能鉴别碳酸钠和碳酸氢钠,
故答案为:Ⅱ;碳酸氢钠与盐酸反应产生的二氧化碳速率快;
(2)实验Ⅲ、Ⅳ相比,IV可以做到一套装置同时进行两个对比实验,而III不能,故选D,
故答案为:D;
(3)碳酸钠直接加热,碳酸氢钠不直接加热,不直接加热的碳酸氢钠能分解而直接加热的碳酸钠不分解更能说明碳酸氢钠不稳定,
故答案为:NaHCO3;
(4)①当石灰水过量时,离子方程式按照碳酸氢钠的组成书写,反应的离子方程式为:HCO3-+OH-+Ca2+═CaCO3↓+H2O,
故答案为:HCO3-+OH-+Ca2+═CaCO3↓+H2O;
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,反应方程式为:2HCO3-+2OH-+Ca2+═CaCO3↓+H2O+CO32-,所以溶液中的溶质是Na2CO3,
故答案为:Na2CO3;
(5)检查各装置气密性的方法为:将导气管末端插入水中,然后用手握住或利用热毛巾捂容器对该仪器装置微热,观察导管末端有气泡逸出,且松开手后,观察到导管末端形成一段水柱,说明气密性好,
故答案为:将导气管末端插入水中,然后用手握住或利用热毛巾捂容器对该仪器装置微热,导管末端有气泡逸出,且松开手后,观察到导管末端形成一段水柱,说明气密性好.
点评:本题考查了碳酸钠和碳酸氢钠的性质,题目难度中等,熟练掌握掌握碳酸钠、碳酸氢钠的化学性质为解答关键,试题培养了学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
某温度下,向2L恒容密闭容器中充入1.0mol A和1.0mol B,反应A(g)+B(g)?C(g)经过一段时间后达到平衡.反应过程中测定的部分数据见下表,下列说法正确的是( )
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A、反应在前5 s的平均速率v(A)=0.17 mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时c(A)=0.41 mol?L-1,则反应的△H>0 |
| C、相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80% |
| D、相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆) |
(双选)有两种金属混合粉末15g,加入足量的稀盐酸充分反应后,得到11.2LH2(标准状况),则下列各组金属中肯定不能构成上述混合物的是( )
| A、Mg、Al |
| B、Mg、Cu |
| C、Cu、Zn |
| D、Al、Fe |


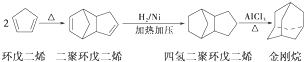
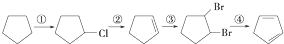
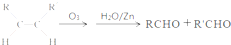 .请写出下列反应产物的结构简式:
.请写出下列反应产物的结构简式: