题目内容
有A、B、C、D四种无色可溶性盐分别是由Na+、Mg2+、Ag+、Ba2+、Cl-、CO32-、HCO3-、NO3-中不同的阴阳离子所组成.A溶液与硫酸反应只有气体生成,B溶液与硫酸反应只有沉淀生成,C溶液与硫酸反应既有气体又有沉淀生成,D溶液与硫酸反应既无气体又无沉淀生成,则
(1)A为 、B为 、C为 、D为 (均写化学式)
(2)分别写出下列反映的三个离子方程式
①A与足量的硫酸溶液 ;
②C与足量的硫酸溶液 ;
③C与少量的氢氧化钠溶液 .
(1)A为
(2)分别写出下列反映的三个离子方程式
①A与足量的硫酸溶液
②C与足量的硫酸溶液
③C与少量的氢氧化钠溶液
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:给出八种离子形成四种可溶性盐,这个可以通过一一组合的形式确定可能存在的物质,之后结合实验现象进行继续排除,从而最终确定.A溶液与稀硫酸混合产生无色无味的气体,说明A中含有CO32-或HCO3-,B溶液与稀硫酸混合产生沉淀,则说明B中含有Ag+或Ba2+,C溶液与硫酸反应有气体生成说明含CO32-或HCO3-、又有沉淀生成,说明含Ag+或Ba2+,结合C可溶可知C为Ba(HCO3)2;Ag+和Cl-、CO32-均生成沉淀,故B为和AgNO3;Mg2+和CO32-反应生成沉淀,故A为Na2CO3,D为MgCl2,据此答题.
解答:
解:(1)给出八种离子形成四种可溶性盐,这个可以通过一一组合的形式确定可能存在的物质,之后结合实验现象进行继续排除,从而最终确定.A溶液与稀硫酸混合产生无色无味的气体,说明A中含有CO32-或HCO3-,B溶液与稀硫酸混合产生沉淀,则说明B中含有Ag+或Ba2+,C溶液与硫酸反应有气体生成说明含CO32-或HCO3-、又有沉淀生成,说明含Ag+或Ba2+,结合C可溶可知C为Ba(HCO3)2;Ag+和Cl-、CO32-均生成沉淀,故B为和AgNO3;Mg2+和CO32-反应生成沉淀,故A为Na2CO3,D为MgCl2.
故答案为:Na2CO3;AgNO3;Ba(HCO3)2;MgCl2;
(2)Na2CO3 与硫酸反应生成硫酸钠、二氧化碳和水,反应的离子方程式为:2H++CO32-=H2O+CO2↑;
Ba(HCO3)2 和硫酸反应生成硫酸钡、二氧化碳和水,反应的离子方程式为:2H++SO42-+2HCO3-+Ba2+=BaSO4↓+2H2O+2CO2↑;
Ba(HCO3)2 和少量氢氧化钠反应,由于钡离子过量,故生成碳酸钡和水,反应的离子方程式为:OH-+HCO3-+Ba2+=BaCO3↓+H2O;
故答案为:2H++CO32-=H2O+CO2↑;2H++SO42-+2HCO3-+Ba2+=BaSO4↓+2H2O+2CO2↑;OH-+HCO3-+Ba2+=BaCO3↓+H2O.
故答案为:Na2CO3;AgNO3;Ba(HCO3)2;MgCl2;
(2)Na2CO3 与硫酸反应生成硫酸钠、二氧化碳和水,反应的离子方程式为:2H++CO32-=H2O+CO2↑;
Ba(HCO3)2 和硫酸反应生成硫酸钡、二氧化碳和水,反应的离子方程式为:2H++SO42-+2HCO3-+Ba2+=BaSO4↓+2H2O+2CO2↑;
Ba(HCO3)2 和少量氢氧化钠反应,由于钡离子过量,故生成碳酸钡和水,反应的离子方程式为:OH-+HCO3-+Ba2+=BaCO3↓+H2O;
故答案为:2H++CO32-=H2O+CO2↑;2H++SO42-+2HCO3-+Ba2+=BaSO4↓+2H2O+2CO2↑;OH-+HCO3-+Ba2+=BaCO3↓+H2O.
点评:本题主要考查了溶液中离子共存的问题,要注意元素化合物知识的灵活运用,题目难度不大.易错点为Ba(HCO3)2 和少量氢氧化钠反应离子方程式的书写,注意量不同,离子方程式不同.

练习册系列答案
相关题目
如图是立方烷的键线式结构,下列有关说法不正确的是( )
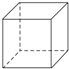

| A、它和苯的最简式相同 |
| B、它属于芳香烃 |
| C、它只有两种化学键 |
| D、它与苯乙烯(C6H5-CH═CH2)具有相同的分子式 |
下列叙述正确的是( )
| A、金属氧化物一定是碱性氧化物 |
| B、非金属氧化物一定是酸性氧化物 |
| C、只有在标准状况下,气体的摩尔体积才能为22.4L/mol |
| D、非电解质在水溶液中和熔融状态下均以分子形式存在,因而不能导电 |
下列说法不正确的是( )
| A、检验食盐中含有钠离子,可以用焰色反应实验,如果焰色呈黄色则可以说明含有钠离子 |
| B、检验食盐中含有氯离子,则可以加用硝酸酸化的硝酸银溶液 |
| C、向溴水中加入食盐溶液,可以使溴水褪色 |
| D、食盐中加碘的作用是预防“大脖子病”的发生 |
25℃,101k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为-57.3kJ?mol-1,辛烷的标准燃烧热为-5518kJ?mol-1.下列热化学方程式书写正确的是( )
| A、2H+(aq)+SO42- (aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l)△H=-114.6 kJ?mol-1 | ||
| B、2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l)△H=-57.3 kJ?mol-1 | ||
C、C8H18(1)+
| ||
D、C8H18(g)+
|