题目内容
等质量的两份锌粉a、b,分别加入两支相同的试管中,然后加入等体积等物质的量浓度且均过量的稀硫酸,同时向a中加入少量CuSO4溶液,则产生氢气的体积(V)与时间(t)的关系用图象表示如下,其中正确的是( )
A、 |
B、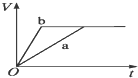 |
C、 |
D、 |
考点:化学反应速率的影响因素
专题:
分析:在a中加入加入少量CuSO4溶液,锌置换出铜可形成铜锌原电池,由于稀硫酸过量,生成的氢气不相等,以此解答该题.
解答:
解:在a中加入少量CuSO4溶液,锌置换出铜可形成铜锌原电池,反应速率增大,由于酸过量,则锌完全反应,加入硫酸铜的a生成氢气体积小、速率快,b生成氢气速率慢、体积大,所以只有D符合.
故选D.
故选D.
点评:本题考查化学反应速率的影响因素,为高考高频考点,侧重于学生的分析能力的考查,注意原电池原理能够加快反应速率的特点以及硫酸过量的信息,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目
NA为阿伏加德罗常数,下列叙述正确的是( )
| A、标况下,2.8 L丙烷中含有的极性共价键数为NA |
| B、在反应KIO3+6HI=KI+3I2+3H2O 中,每生成3 mol I2转移的电子数为6 NA |
| C、已知CH3COONH4溶液的PH=7,则1L 0.1mol/L的CH3COONH4溶液中,CH3COO-数为0.1NA |
| D、39g Na2O2和Al(OH)3的混合物中阴、阳离子的总数为2NA |
现有甲、乙、丙、丁四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:甲<丙<乙<丁
Ⅱ.原子的最外层电子数:甲+丙=乙+丁=8
Ⅲ.原子的核外电子层数:丁>乙=丙=2甲
Ⅳ.乙元素的主要化合价:最高正价+最低负价=2
则下列说法不正确的是( )
Ⅰ.原子半径:甲<丙<乙<丁
Ⅱ.原子的最外层电子数:甲+丙=乙+丁=8
Ⅲ.原子的核外电子层数:丁>乙=丙=2甲
Ⅳ.乙元素的主要化合价:最高正价+最低负价=2
则下列说法不正确的是( )
| A、乙元素的最外层有5个电子,其氢化物含有极性键 |
| B、四种元素中丙的非金属性最强,其最高价氧化物对应的含氧酸酸性最强 |
| C、丁元素的氧化物对应的水化物与乙元素最高价氧化物对应水化物恰好完全反应形成的盐溶液显酸性 |
| D、乙、丙两元素形成的简单氢化物稳定性丙的强于乙 |
向10ml某浓度的盐酸中逐渐加入0.1mol/L氨水,溶液的pH与加入的氨水的体积关系曲线如图所示,下列各项中正确的是( )

| A、盐酸浓度为 1 mol/L |
| B、在B点:c(NH4+)=c(Cl -)>c(OH -)=c(H+),且a>10 |
| C、在A、B间任意一点:c(Cl -)>c(NH4+)>c(H+)>c(OH -) |
| D、在C点:c(NH4+)>c(Cl -)>c(H+)>c(OH -) |
某温度下,将2 molA 和2 molB放入2L密闭容器中,发生反应:A(g)+B(g)?2C(s)=2D(g)△H<0,5min后应达到平衡,测得生成C为0.8mol,下列相关表述正确的是( )
| A、该反应的化学平衡常数为K=0.04 |
| B、若向平衡体系中加入少量生成物A,则A和B的转化率均增大 |
| C、若混合气体的平均摩尔质量不再随时间变化,说明反应达到了平衡状态 |
| D、若给平衡体系升高温度,则正反应速率瞬间减小,逆反应速率瞬间增大 |
下列鉴别方法不可行的是( )
| A、用水鉴别乙醇、甲苯和溴苯 |
| B、用燃烧法鉴别乙醇、苯和四氯化碳 |
| C、用酸性高锰酸钾溶液鉴别苯、环已烯和环己烷 |
| D、用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )

| A、可以和溴水反应 |
| B、可溶于有机溶剂 |
| C、分子中有三个苯环 |
| D、1mol维生素P最多可以和4molNaOH反应 |