题目内容
8.用NA表示阿伏加德罗常数的值.下列判断正确的是( )| A. | 44g N20含有的氮原子数目为NA | |
| B. | 常温常压下,22.4L N2含有的分子数目为NA | |
| C. | lmol Mg变为Mg2+时失去的电子数目为2NA | |
| D. | 1L lmol•L-1K2CO3,溶液中含有的钾离子数目为NA |
分析 A、求出一氧化二氮的物质的量,然后根据1molN2O中含2mol氮原子来分析;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、镁原子变为镁离子时失去2个电子;
D、求出碳酸钾的物质的量,然后根据1mol碳酸钾中含2mol钾离子来分析.
解答 解:A、44g一氧化二氮的物质的量为1mol,而1molN2O中含2mol氮原子,即含2NA个,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L氮气的物质的量小于1mol,则分子个数小于NA个,故B错误;
C、镁原子变为镁离子时失去2个电子,故1mol镁变为镁离子时失去2NA个电子,故C正确;
D、溶液中碳酸钾的物质的量为n=CV=1mol/L×1L=1mol,而1mol碳酸钾中含2mol钾离子,故含2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
18.卤素是最活泼的一族非金属,下列关于卤族元素的说法正确的是( )
| A. | 卤素单质的最外层电子数都是7 | |
| B. | 卤素单质与H2化合的容易程度为F2<Cl2<Br2<I2 | |
| C. | 卤素单质与H2化合的产物由上至下稳定性减弱,其水溶液的酸性增强 | |
| D. | 从F到I,元素非金属性依次减弱,则其最高价氧化物的水化物的酸依次减弱 |
19.下列说法正确的是( )
| A. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| C. | 在加热条件下发生的反应均为吸热反应 | |
| D. | 物质发生化学反应时不一定都伴随着能量变化 |
16.月球中有大量${\;}_{2}^{3}$He,${\;}_{2}^{3}$He是核聚变的优质材料${\;}_{2}^{3}$He中的“3”是指该原子的( )
| A. | 质子数 | B. | 质量数 | C. | 中子数 | D. | 电子数 |
3.下列化学用语表示正确的是( )
| A. | 乙烯的结构简式:C2H4 | |
| B. | HCl的电子式: | |
| C. | CH3COOH官能团名称:羟基 | |
| D. | 氨水的电离方程式:NH3•H2O?NH${\;}_{4}^{+}$+OH- |
13.锌锰干电池是家庭常用的电池,该电池工作时发生的化学反应为:Zn+2NH4C1+2Mn02═Zn( NH3)2C12+2MnO(OH),下列说法正确的是( )
| A. | 电池工作时锌片作为正极 | |
| B. | 电池工作时从正极向外电路输出电子 | |
| C. | 电池工作时Mn02发生还原反应 | |
| D. | 电池工作时电能向化学能转化 |
17.常温下,有pH=1的某溶液中可能含有Na+、Fe2+、Fe3+、I-、Cl-、CO32-中的某几种,现取100mL该溶液进行如下实验:

根据实验结果,下列判断正确的是( )

根据实验结果,下列判断正确的是( )
| A. | Fe2+、I-、Cl-三种离子一定存在 | |
| B. | 不能确定Na+和Cl-是否存在,CO${\;}_{3}^{2-}$一定不存在 | |
| C. | Fe3+与Fe2+至少有一种 | |
| D. | 该溶液中c(Cl-)≥0.1mol•L-1 |
18.如表是元素周期表中短周期的一部分.已知元素④的最高价氧化物的水化物是两性氢氧化物.
(1)某元素能形成的化合物种类最多,该元素是碳(填名称),位于第二周期IVA族,;
(2)⑤⑥⑦号元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式).画出⑥⑦号元素形成的简单离子的结构示意图: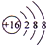 、
、 ,这两种离子的半径大小顺序是S2->Cl-(填化学式).
,这两种离子的半径大小顺序是S2->Cl-(填化学式).
(3)②③⑥号元素的氢化物中,沸点最高的是H2O(填化学式);
(4)③④⑥号元素中,原子半径最大的是④(填序号).
| ① | ② | ③ | ||
| ④ | ⑤ | ⑥ | ⑦ |
(2)⑤⑥⑦号元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式).画出⑥⑦号元素形成的简单离子的结构示意图:
 、
、 ,这两种离子的半径大小顺序是S2->Cl-(填化学式).
,这两种离子的半径大小顺序是S2->Cl-(填化学式).(3)②③⑥号元素的氢化物中,沸点最高的是H2O(填化学式);
(4)③④⑥号元素中,原子半径最大的是④(填序号).