题目内容
5.甲醇是一种重要的化工原料,在化工领域有广泛应用.(1)由合成气(组成为H2、CO和少量CO2)直接制备甲醇,其主要过程包括以下2个反应:
Ⅰ、CO(g)+2H2(g)=CH3OH(g)△H1=-90.1kJ•mol-1
Ⅱ、CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2=-49.0kJ•mol-1
①与反应Ⅱ比较,采用反应Ⅰ制备甲醇的优点是无副产物生成,原子利用率高.
②CO(g)与H2O (g)生成CO2(g)和H2(g)的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.1 kJ•mol-1.
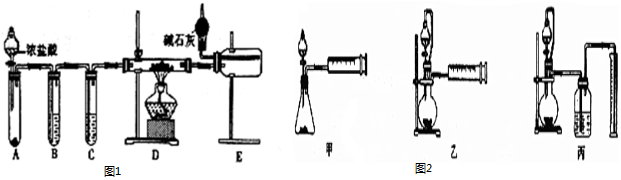
③图1示意图中,能正确表示利用反应Ⅱ原理制备甲醇的反应过程中能量变化的是A(填序号).

(2)甲醇燃料电池由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.其工作原理如图2所示:
①负极的电极反应式为CH3OH-6e-+H2O=CO2+6H+.
②若该电池中消耗6.4g甲醇,则转移1.2mol电子.
(3)污水中的含氮化合物,通常先用生物膜脱氮工艺进行处理,在硝化细菌的作用下将NH4+最终氧化为HNO3,然后加入CH3OH,得到两种无毒气体.写出加入CH3OH后发生反应的离子方程式6NO3-+5CH3OH+6H+=3N2↑+5CO2↑+13H2O.
分析 (1)①从原子利用率角度来解答;
②Ⅰ、CO(g)+2H2(g)=CH3OH(g)△H1=-90.1kJ•mol-1
Ⅱ、CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2=-49.0kJ•mol-1,Ⅰ-Ⅱ得,CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.1 kJ•mol-1,据此进行分析;
③根据②中分析可知,正反应为放热反应,则反应物总能量大于生成物总能量,由于气态物质的能量高于液态物质,故生成液态产物放出的热量更多;
(2)①甲醇燃料电池,电解质为酸,由氢离子向正极移动可知,a为负极,甲醇失去电子发生氧化反应,据此书写电极反应方程式;
②结合电极反应及转移电子计算;
(3)据题意书写离子方程式.
解答 解:(1)①相对反应A,采用反应B制备甲醇的优点是原子利用率为100%,符合原子经济和绿色化学的思想,
故答案为:无副产物生成,原子利用率高;
②Ⅰ、CO(g)+2H2(g)=CH3OH(g)△H1=-90.1kJ•mol-1
Ⅱ、CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2=-49.0kJ•mol-1,Ⅰ-Ⅱ得,CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.1 kJ•mol-1,
故答案为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.1 kJ•mol-1;
③根据②中分析可知,正反应为放热反应,则反应物总能量大于生成物总能量,由于气态物质的能量高于液态物质,故生成液态产物放出的热量更多,图象中A符合,
故答案为:A;
(2)①根据图知,交换膜是质子交换膜,则电解质溶液呈酸性,根据氢离子移动方向知,通入a的电极为负极、通入b的电极为正极,负极上甲醇失去电子发生氧化反应,负极反应式为 CH3OH-6e-+H2O=CO2+6H+,
故答案为:CH3OH-6e-+H2O=CO2+6H+;
②6.4g甲醇相当于$\frac{6.4g}{32g/mol}$=0.2mol甲醇,据电极反应方程式CH3OH-6e-+H2O=CO2+6H+,1molCH3OH转移6mol电子,故0.2molCH3OH转移1.2mol电子,
故答案为:1.2;
(3)在硝化细菌的作用下将NH4+最终氧化为HNO3,然后加入CH3OH,得到两种无毒气体,故加入CH3OH后发生反应的离子方程式6NO3-+5CH3OH+6H+=3N2↑+5CO2↑+13H2O,
故答案为:6NO3-+5CH3OH+6H+=3N2↑+5CO2↑+13H2O.
点评 本题考查了热化学方程式的书写、燃料电池电极反应式的书写以及氧化还原反应的书写,本题难度中等.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. | 标准状况下5.6L CH4含有的共用电子对数目为NA | |
| B. | 25℃时,pH=1的硫酸溶液中含有H+的数目为0.1NA | |
| C. | 常温下,23g NO2和N2O4混合气体中所含原子总数为1.5NA | |
| D. | 将0.5mol NH4NO3于稀氨水使溶液呈中性,溶液中NH4+数目为0.5NA |
| A. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA | |
| B. | 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA | |
| C. | 标准状况下,44.8L NO与22.4 L O2反应后的分子数是2NA | |
| D. | 27g铝中加入1mol/L的NaOH溶液,转移电子数是3NA |
(1)已知:
CH3OH(g)=HCHO(g)+H2(g)△H=+84kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g)△H=-316 kJ•mol-1.
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)?CH3OH(g),已知某些化学键的键能数据如表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | O-H |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | x | 463 |
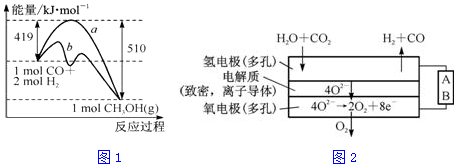
①该反应的△S<(填“>”或“<”)0.图1中曲线a到曲线b的措施是加入催化剂.
②已知CO中的C与O之间为三键,其键能为x kJ•mol-1,则x=1097.
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如表离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42 - |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
(4)电解水蒸气和CO2产生合成气(H2+CO).较高温度下(700~1 000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2.由图2可知A为直流电源的负极(填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:H2O+2e-=H2↑+O2-.
| A. | 如图的键线式表示烃的名称为3-甲基-4-乙基-7-甲基辛烷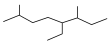 | |
| B. | 符合分子式为C3H8O的醇有三种不同的结构 | |
| C. | 乙烯在一定条件下能发生加成反应、加聚反应,被酸性高锰酸钾溶液氧化,也能在一定条件下被氧气氧化成乙酸 | |
| D. | 溴水能将 甲苯、乙烯、乙醇、四氯化碳、乙酸五种溶液鉴别开来 |
| A. | 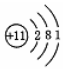 | B. | 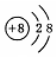 | C. | 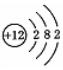 | D. | 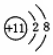 |
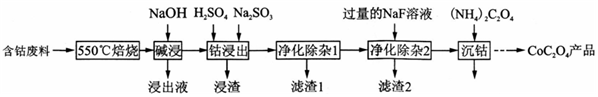
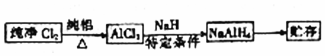
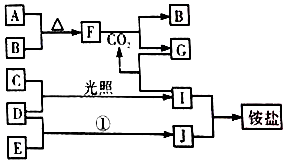 如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要固氮反应
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要固氮反应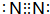 ,F
,F ;
; ;
;