题目内容
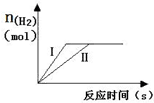 如图表示相同质量的Mg、Al分别跟一定量的稀H2SO4溶液反应的情况,下列叙述可能符合图示的是( )
如图表示相同质量的Mg、Al分别跟一定量的稀H2SO4溶液反应的情况,下列叙述可能符合图示的是( )| A、Mg、Al均不足,H2SO4过量 |
| B、消耗稀H2SO4的量是Ⅱ大于Ⅰ |
| C、Ⅰ表示Mg与稀H2SO4反应 |
| D、产生H2的速率是Ⅱ大于Ⅰ |
考点:镁的化学性质,铝的化学性质
专题:元素及其化合物
分析:镁比铝活泼,与稀硫酸反应时速率较快;反应的化学方程式分别为Mg+H2SO4═MgSO4+H2↑、2Al+3H2SO4═Al2(SO4)3+3H2↑,生成氢气相同,则消耗的硫酸相同,镁和铝应过量,以此解答.
解答:
解:镁比铝活泼,与稀硫酸反应时速率较快,则曲线Ⅰ表示Mg与稀H2SO4反应,曲线Ⅱ表示Al与稀H2SO4反应,故C正确,D错误;
反应的化学方程式分别为Mg+H2SO4═MgSO4+H2↑、2Al+3H2SO4═Al2(SO4)3+3H2↑,如金属完全反应,则生成氢气的物质的量不同,由图象可知,生成氢气相同,则消耗的硫酸相同,镁和铝应过量,故AB错误;
故选C.
反应的化学方程式分别为Mg+H2SO4═MgSO4+H2↑、2Al+3H2SO4═Al2(SO4)3+3H2↑,如金属完全反应,则生成氢气的物质的量不同,由图象可知,生成氢气相同,则消耗的硫酸相同,镁和铝应过量,故AB错误;
故选C.
点评:本题主要考查镁、铝的性质,侧重于学生的计算和判断能力的考查,要充分利用图中提供的信息进行分析、判断,从而得出正确的结论,难度不大.

练习册系列答案
相关题目
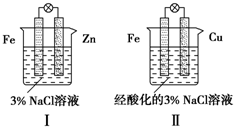 K3[Fe(CN)6]铁氰化钾,别名赤血盐,深红色或红色单斜晶系柱状结晶或粉未,有剧毒.遇亚铁盐生成蓝色沉淀.结合下图判断,下列叙述正确的是( )
K3[Fe(CN)6]铁氰化钾,别名赤血盐,深红色或红色单斜晶系柱状结晶或粉未,有剧毒.遇亚铁盐生成蓝色沉淀.结合下图判断,下列叙述正确的是( )| A、Ⅰ和Ⅱ中负极反应均是Fe-2e-═Fe2+ |
| B、Ⅰ和Ⅱ中正极均被保护 |
| C、Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-═4OH- |
| D、Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀 |
能证明Al2O3属离子化合物的是( )
| A、熔融时能导电 |
| B、可作耐火材料 |
| C、受热难分解 |
| D、能溶于NaOH溶液 |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达正确的是( )
A、Fe在Cl2中的燃烧产物: |
B、Na与O2反应的产物: |
C、AlCl3溶液中滴加氨水后铝的存在形式: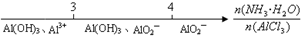 |
D、NaAlO2溶液中滴加盐酸后铝的存在形式: |
下列应用特征现象推断不正确的是( )
| A、遇FeCl3溶液显紫色或加入溴水产生白色沉淀,表示物质中可能含有酚羟基 |
| B、加入新制Cu(OH)2悬浊液并加热,有红色沉淀生成,或加入银氨溶液并水浴加热有银镜出现,说明该物质中含有-CHO |
| C、加入金属钠,有H2产生,表示物质可能有-OH或-COOH |
| D、加入NaHCO3溶液有气体放出或能使紫色石蕊试液变红,表示物质中含有-COOH |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、25℃时,1 L 0.1 mol?L-1的CH3COOH溶液中,含氢离子数约为0.1NA |
| B、标准状况下,22.4 L CHCl3中含氯原子数为3NA |
| C、1mol Na2O2晶体中所含离子数为3NA |
| D、0.5 mol NaCl晶体中含0.5NA个NaCl分子 |
丁腈橡胶( )具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
)具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
①CH2═CH-CH═CH2 ②CH3-CH═CH-CH3 ③CH2═CH-CN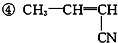 ⑤CH3-CH═CH2.
⑤CH3-CH═CH2.
 )具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
)具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )①CH2═CH-CH═CH2 ②CH3-CH═CH-CH3 ③CH2═CH-CN
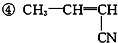 ⑤CH3-CH═CH2.
⑤CH3-CH═CH2.| A、③⑤ | B、②③ | C、①③ | D、④⑤ |