题目内容
7.足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入4mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,下列说法正确的是( )| A. | 消耗氧气的体积为1.68 L | |
| B. | 混合气体中含NO21.12 L | |
| C. | 此反应过程中转移的电子为0.3 mol | |
| D. | 参加反应的硝酸是0.4mol |
分析 标况下2.24L混合气体的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,则n(NO2)+n(NO)=0.1,得失电子守恒知:n(NO2)+3n(NO)=0.2,4mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,反应消耗的铜的物质的量为4mol•L-1×50×10-3L×$\frac{1}{2}$=0.1mol,0.1mol铜完全反应失去0.2mol电子,根据电子守恒,氧气得到的电子与铜失去的电子一定相等,根据电子守恒计算出消耗氧气物质的量,由此分析解答.
解答 解:标况下2.24L混合气体的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,则n(NO2)+n(NO)=0.1,得失电子守恒知:n(NO2)+3n(NO)=0.2,解得n(NO2)=0.05mol,n(NO)=0.05mol,4mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,反应消耗的铜的物质的量为4mol•L-1×50×10-3L×$\frac{1}{2}$=0.1mol,0.1mol铜完全反应失去0.2mol电子,
A、消耗氧气的体积为$\frac{0.2}{4}$×22.4=1.12 L,故A错误;
B、因为n(NO2)=0.05mol,所以V(NO2)=0.05mol×22.4L/mol=1.12 L,故B正确;
C、此反应过程中转移的电子为0.2 mol,故C错误;
D、参加反应的硝酸是0.1mol+0.2mol=0.3mol,故D错误;
故选B.
点评 本题考查了有关离子反应的计算,题目难度中等,明确铜过量及发生反应原理为解答关键,转移电子守恒、质量守恒在化学计算中的应用方法.

| A. | NaHCO3能与碱反应,可用作焙制糕点的膨松剂 | |
| B. | 液氨汽化时吸收大量的热,可用作制冷剂 | |
| C. | 硅酸钠溶液呈碱性,可用作木材防火剂 | |
| D. | Fe比Cu活泼,可用FeCl3溶液腐蚀线路板上的Cu |
| A. | 阴极增重1.72g | B. | 所得溶液 pH<1 | C. | 阴极增重0.64g | D. | 所得溶液pH>1 |
| A. | 标准状况下,22.4 L NH3溶于水后溶液中含有NA个NH4+ | |
| B. | 1L 0.1 mol•L-1的Na2CO3溶液中含有0.2 NA个Na+ | |
| C. | 1 mol 硫酸钾中阴离子所带电荷数为NA | |
| D. | 将0.1mol氯化铁溶于1L水中,所得溶液中含有0.1NAFe3+ |
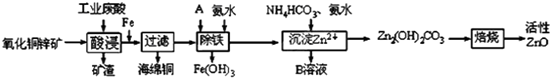
已知:各离子开始沉淀及完全沉淀时的pH如下表所示.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是适当升高温度(或增大酸浓度、将氧化铜锌矿粉碎等).(任写一点即可)
(2)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,
则相同温度下:Ksp(CuS)<Ksp(ZnS)(选填“>”“<”或“=”).
(3)物质A是用来将ZnSO4溶液中的Fe2+转化为Fe3+最好使用下列物质中的B.
A.KMnO4B.H2O2 C.HNO3 D.NaClO
(4)除铁过程中加入氨水的目的是通过调节溶液的pH,使Fe3+沉淀而Zn2+不沉淀,pH应控制在3.2≤pH<6.2或3.2~6.2范围之间.
(5)物质B可直接用作氮肥,则B的化学式是(NH4)2SO4.
(6)写出最后焙烧生成ZnO的化学反应方程式Zn2(OH)2CO3=2ZnO+H2O+CO2↑.
| A. | NaH在水中显碱性 | |
| B. | NaH中氢离子电子层排布与氦原子相同 | |
| C. | NaH中氢离子半径比锂离子半径大 | |
| D. | NaH中氢离子被还原为H2 |
| A. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增多 | |
| B. | 有气体参加的反应,若增大压强,可增大活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能使反应速率增大的主要原因是减小了反应物分子中活化分子的百分数 | |
| D. | 催化剂能增大活化分子的百分数,从而成千上万倍地增大反应速率 |
| A. | X、Y、Z、W 元素的离子半径依次减小 | |
| B. | W 的气态氢化物的沸点一定高于Z的气态氢化物的沸点 | |
| C. | 若W 与Y的原子序数相差5,则二者形成的化合物的化学式可能为Y2W3或Y3W2 | |
| D. | W 与X形成的化合物只含离子键 |