题目内容
取agNa2O2与Al粉组成的混合物,投入足量的水中,固体完全溶解,
求(1)在标况下放出气体V L(设产生的气体全部放出) 的取值范围.
(2)若VL气体点燃时恰好完全反应,则原混合物中过氧化钠与铝物质的量之比为?
求(1)在标况下放出气体V L(设产生的气体全部放出) 的取值范围.
(2)若VL气体点燃时恰好完全反应,则原混合物中过氧化钠与铝物质的量之比为?
考点:有关范围讨论题的计算,有关混合物反应的计算
专题:
分析:(1)Na2O2与Al粉组成的混合物,放入适量的水中,固体完全溶解,根据反应2Na2O2+2H2O═4NaOH+O2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,过氧化钠的物质的量与Al的物质的量之比大于或等于1:2,据此根据极限法计算;
(2)氢气与氧气完全燃烧的物质的量之比为2:1,据此解答即可.
(2)氢气与氧气完全燃烧的物质的量之比为2:1,据此解答即可.
解答:
解:(1)若Al和Na2O2与水反应生成的NaOH恰好反应.根据反应2Na2O2+2H2O═4NaOH+O2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,过氧化钠的物质的量与Al的物质的量之比等于1:2,令过氧化钠的物质的量为xmol,则铝为2xmol,所以78x+54x=a,解得x=
.所以生成气体为:
2Na2O2+2H2O═4NaOH+O2↑,
2 1
mol
×
mol
2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
2 3
2×
mol 3×
mol
所以生成的气体体积为(
×
mol+3×
mol)×22.4L/mol=
L,
若只有过氧化钠,ag过氧化钠的物质的量为
=
mol,生成气体为:
2Na2O2+2H2O═4NaOH+O2↑
2 1
mol
×
mol,所以生成气体体积为
×
mol×22.4L/mol=
L,所以气体体积V的取值范围为
<V≤
,
答:在标况下放出气体V L(设产生的气体全部放出) 的取值范围为
<V≤
;
(2)若V L气体点燃时恰好完全反应,则n(O2):n(H2)=1:2,由方程式可知,n(2Na2O2):n(Al)=3:2,
答:原混合物中过氧化钠与铝物质的量之比为3:2.
| a |
| 132 |
2Na2O2+2H2O═4NaOH+O2↑,
2 1
| a |
| 132 |
| 1 |
| 2 |
| a |
| 132 |
2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
2 3
2×
| a |
| 132 |
| a |
| 132 |
所以生成的气体体积为(
| 1 |
| 2 |
| a |
| 132 |
| a |
| 132 |
| 156.8a |
| 264 |
若只有过氧化钠,ag过氧化钠的物质的量为
| ag |
| 78g/mol |
| a |
| 78 |
2Na2O2+2H2O═4NaOH+O2↑
2 1
| a |
| 78 |
| 1 |
| 2 |
| a |
| 78 |
| a |
| 78 |
| 1 |
| 2 |
| 22.4a |
| 156 |
| 22.4a |
| 156 |
| 156.8a |
| 264 |
答:在标况下放出气体V L(设产生的气体全部放出) 的取值范围为
| 22.4a |
| 165 |
| 156.8a |
| 264 |
(2)若V L气体点燃时恰好完全反应,则n(O2):n(H2)=1:2,由方程式可知,n(2Na2O2):n(Al)=3:2,
答:原混合物中过氧化钠与铝物质的量之比为3:2.
点评:本题考查混合物的计算,难度较大,清楚反应过程注意根据反应的有关化学方程式进行计算,固体完全溶解,根据反应2Na2O2+2H2O═4NaOH+O2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑判断过氧化钠的物质的量与Al的物质的量之比大于或等于1:2是关键.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
 是存在于石油中的一种烃,其裂解时可能发生的反应如下,下列说法中正确的是( )
是存在于石油中的一种烃,其裂解时可能发生的反应如下,下列说法中正确的是( )
| A、M为H2,N为C5H8 |
B、在 和 和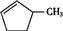 的混合物中加入溴水,分液得到 的混合物中加入溴水,分液得到 |
C、等质量的 和 和 完全燃烧消耗氧气的量 完全燃烧消耗氧气的量 多 多 |
| D、产物C4H6不可能是炔烃 |
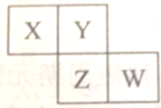 XYZW均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的
XYZW均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的| 7 |
| 10 |
| A、阴离子的半径从大到小的排列顺序为X>Y>Z>W |
| B、X元素的氢化物分子间可形成氢键 |
| C、Y的两种同素异形体在一定条件下可以相互转化 |
| D、最高价氧化物对应的水化物的酸性:W>Z |
下列为制取溴苯实验的有关现象的解释和叙述中正确的是( )
| A、实验室制取的溴苯为褐色的液体,是其中液溴造成的 |
| B、溴苯比水轻,因此溴苯浮在水面上 |
| C、实验室制取溴苯时,导管口出现白雾,是由于HBr遇水蒸气而形成的 |
| D、溴苯和苯的混合物可以用水萃取分离 |