��Ŀ����
��6�֣�ˮ��Һ�д��ڶ���ƽ�⣬�������ѧ��ѧ֪ʶ�ش��������⣺
��1����Ũ�Ⱦ�Ϊ0.1mol/L��CH3COONH4 ��NH4HSO4 ��NH3.H2O ��(NH4)2SO4��Һ�У�NH4+Ũ���ɴ�С��˳��Ϊ ������ţ�
��2��Ũ�Ⱦ�Ϊ0.1 mol��L��1��������Һ�������ᡢ�ڴ��ᡢ���������ơ����Ȼ��������Һ����ˮ�������H��Ũ���ɴ�С��˳����(�����) ��
��3�������£���pH=6������ˮ�м���2.3g�����ƣ���ַ�Ӧ���ټ�����ˮϡ�͵�1L��������Һ��pH= ��
��1����>��>��>�ۣ���2����>��>��>�٣���3��11
��������
������������������ʵ���Һ�д��ڵĴ�������ʽ�ǣ���CH3COONH4= CH3COO-+NH4+����NH4HSO4=NH4++H++SO42-����NH3.H2O NH4++OH-����(NH4)2SO4= 2NH4++ SO42-���ڢ٢ڢ��ж�����NH4+����ˮ�ⷴӦ�Ķ�����ʹ���ӵ�Ũ�ȼ�С����CH3COO-��ǰ����ٽ����ã�ʹ����Ũ�Ƚ�һ����С����H+��NH4+����ˮ�ⷴӦ���������ã����Ԣ�>��.���������غ��֪��>�ڣ�NH3.H2O��������ʣ�����̶������ģ�����������Ũ��ԶС���ε������������Ũ�ȣ���ˢ�>�ۡ���������Һ�е�����Ũ�ȹ�ϵ���Ǣ�>��>��>�ۣ���2���������Ƕ�Ԫǿ�ᣬ��ȫ���룻������������һԪǿ���ȫ����ڴ�����һԪ���ᣬ���ֵ��룬���Dz��������Ӷ�ˮ�ĵ������������ã��������������Ũ��Խ��ˮ�ĵ�����������þ�Խ�����Զ�ˮ���������â�>��>�ڣ����Ȼ����ǿ�������Σ����������NH4+����ˮ�ⷴӦ����ˮ���������OH-����ٽ�ˮ�ĵ������á�������ˮ�������H��Ũ���ɴ�С��˳���Ǣ�>��>��>�٣���3�������£���pH=6������ˮ�м���2.3g�����ƣ�n(OH-)=0.1mol��c(OH-)=0.1mol/L,������������Һ��pH=6�������ڸ��¶��µ�ˮ�����ӻ���������1��10-12��c(H+)=1��10-12��0.1mol/L=1��10-11,���Գ�ַ�Ӧ���ټ�����ˮϡ�͵�1L��������Һ��pH=11.
NH4++OH-����(NH4)2SO4= 2NH4++ SO42-���ڢ٢ڢ��ж�����NH4+����ˮ�ⷴӦ�Ķ�����ʹ���ӵ�Ũ�ȼ�С����CH3COO-��ǰ����ٽ����ã�ʹ����Ũ�Ƚ�һ����С����H+��NH4+����ˮ�ⷴӦ���������ã����Ԣ�>��.���������غ��֪��>�ڣ�NH3.H2O��������ʣ�����̶������ģ�����������Ũ��ԶС���ε������������Ũ�ȣ���ˢ�>�ۡ���������Һ�е�����Ũ�ȹ�ϵ���Ǣ�>��>��>�ۣ���2���������Ƕ�Ԫǿ�ᣬ��ȫ���룻������������һԪǿ���ȫ����ڴ�����һԪ���ᣬ���ֵ��룬���Dz��������Ӷ�ˮ�ĵ������������ã��������������Ũ��Խ��ˮ�ĵ�����������þ�Խ�����Զ�ˮ���������â�>��>�ڣ����Ȼ����ǿ�������Σ����������NH4+����ˮ�ⷴӦ����ˮ���������OH-����ٽ�ˮ�ĵ������á�������ˮ�������H��Ũ���ɴ�С��˳���Ǣ�>��>��>�٣���3�������£���pH=6������ˮ�м���2.3g�����ƣ�n(OH-)=0.1mol��c(OH-)=0.1mol/L,������������Һ��pH=6�������ڸ��¶��µ�ˮ�����ӻ���������1��10-12��c(H+)=1��10-12��0.1mol/L=1��10-11,���Գ�ַ�Ӧ���ټ�����ˮϡ�͵�1L��������Һ��pH=11.
���㣺�����ε�ˮ�⡢Ӱ��ˮ�ĵ���ĸ������أ�ˮ�����ӻ���������Һ��pH�ļ����֪ʶ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�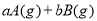
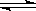
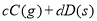
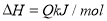 ����Ӧ�����У���������������ʱ��C�ڻ�����еĺ������¶ȣ�T���Ĺ�ϵ��ͼI��ʾ����Ӧ���ʣ�v����ѹǿ��p���Ĺ�ϵ��ͼII��ʾ����ͼ����������˵����ȷ���ǣ�������
����Ӧ�����У���������������ʱ��C�ڻ�����еĺ������¶ȣ�T���Ĺ�ϵ��ͼI��ʾ����Ӧ���ʣ�v����ѹǿ��p���Ĺ�ϵ��ͼII��ʾ����ͼ����������˵����ȷ���ǣ�������