题目内容
5.取25克两种金属 的合金,与足量的盐酸反应,生成氢气2克,组成合金的金属是( )| A. | Al 和Mg | B. | K和 Na | C. | Na 和Al | D. | Zn 和Fe |
分析 2g氢气的物质的量为:$\frac{2g}{2g/mol}$=1mol,设金属的平均化合价为+2价,则金属的物质的量为1mol,混合金属的平均摩尔质量为:$\frac{27g}{1mol}$=27g/mol,Al转化成+2价的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,的+1价的金属Na、K(设摩尔质量为M)转化成+2价时的摩尔质量为2M,据此进行解答.
解答 解:2g氢气的物质的量为:$\frac{2g}{2g/mol}$=1mol,设金属的平均化合价为+2价,则金属的物质的量为1mol,混合金属的平均摩尔质量为:$\frac{27g}{1mol}$=27g/mol,
A.Al转化成+2价的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,Mg的莫若质量为24g/mol,二者的评价摩尔质量不可能为27g/mol,故A错误;
B.K转化成+2价时的摩尔质量为:39g/mol×2=78g/mol,Na转化成+2的摩尔质量为:23g/mol×2=46g/mol,二者的摩尔质量都大于27g/mol,平均摩尔质量不可能为27g/mol,故B错误;
C.Na转化成+2的摩尔质量为:23g/mol×2=46g/mol,Al转化成+2价的摩尔质量为:$\frac{27g/mol}{3}$×2=18g/mol,二者的平均摩尔质量可以为27g/mol,故C正确;
D.Zn、Fe都是+2价金属,二者摩尔质量分别为65g/mol、56g/mol,其平均摩尔质量不可能为27g/mol,故D错误;
故选C.
点评 本题考查了混合物反应的计算,题目难度不大,明确发生反应原理为解答关键,注意掌握平均值发在化学计算中的应用,试题有利于培养学生的分析能力及化学计算能力.

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案| A. | 0.1NA个H2分子的质量为0.2g | |
| B. | 常温常压下,11.2L氯气所含的原子数目为NA | |
| C. | 32g氧气的体积为22.4L | |
| D. | 体积相同的H2和O2含有相同的分子数 |
| A. | 生铁 | B. | 铝热剂 | C. | 明矾 | D. | 赤铁矿 |
| A. | 2.4g金属镁变成镁离子时失去的电子数目为0.1NA | |
| B. | 2g氢气所含原子数目为NA | |
| C. | 1mol Al3+含有核外电子数为3NA | |
| D. | 17g氨气所含电子数目为10NA |
| A. | 反应热是1 mol物质参加反应时的能量变化 | |
| B. | 当反应放热时△H>0,反应吸热时△H<0 | |
| C. | 任何条件下,化学反应的焓变都等于化学反应的反应热 | |
| D. | 在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓的差值来决定 |
| A. | (CH3)3COH的名称:1,1-二甲基乙醇 | B. | 有机物CH3CH=CHCH2OH的键线式为: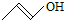 | ||
| C. | 乙醇分子的球棍模型: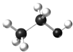 | D. | 氨基的电子式: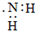 |
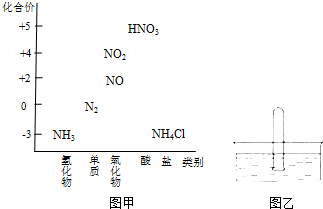 图甲为氮及其化合物的类别与化合价对应的关系图.
图甲为氮及其化合物的类别与化合价对应的关系图. 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.
甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.