题目内容
222 86 |
222 86 |
219 86 |
| A、三种元素 | B、互为同位素 |
| C、同种核素 | D、同一原子 |
考点:质量数与质子数、中子数之间的相互关系,元素,核素,同位素及其应用
专题:
分析:元素的种类由质子数决定;
同位素:质子数相同中子数不同的同一元素互称同位素,
核素的种类由质子数和中子数决定;
原子的种类由质子数和中子数决定;
据此进行分析判断.
同位素:质子数相同中子数不同的同一元素互称同位素,
核素的种类由质子数和中子数决定;
原子的种类由质子数和中子数决定;
据此进行分析判断.
解答:
解:
Rn、
Rn、
Rn是同种元素的不同核素,质子数相同,中子数不同,互为同位素,故选B.
222 86 |
222 86 |
219 86 |
点评:本题考查同位素的概念及判断,同位素是指具有相同质子数,不同中子数同一元素的不同核素,即同一元素的不同原子间互为同位素,注意形似概念的区别.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
| A、相同浓度的两溶液中c(H+)相同 |
| B、100 mL 0.1 mol/L的两溶液分别与氢氧化钠反应至恰好呈中性,盐酸需要的氢氧化钠的物质的量多 |
| C、pH=3的两溶液稀释100倍,醋酸pH变化大 |
| D、两溶液中分别加入少量对应的钠盐固体,c(H+)均明显减小 |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、33.6升CO2与O2的混合气中,含有的氧原子数为3 NA |
| B、15克甲基正离子(CH3+)含有的电子数为8NA |
| C、1molCl2与任何物质充分作用,转移电子数都为2NA |
| D、将0.1 mol N2和0.3 mol H2置于密闭容中充分反应,可得0.2NA个NH3分子 |
下列说法不正确的是( )
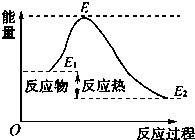

| A、反应物分子间的有效碰撞是反应的先决条件 |
| B、反应物的分子的每次碰撞都能发生化学反应 |
| C、活化分子具有比普通分子更高的能量 |
| D、如图所示正反应的活化能为E-E 1 |
下列有相关说法不正确的是( )
| A、某吸热反应能自发进行,因此该反应是熵增反应 |
| B、在任何条件下,纯水都呈中性 |
| C、水的离子积常数Kw随温度、外加酸(碱)浓度的改变而改变 |
| D、铅蓄电池充电时,标有“-”的电极应与电源的负极相连 |
下列表达式书写正确的是( )
| A、CaCO3的电离方程式:CaCO3?Ca2++CO32- |
| B、HCO3-的水解方程式:HCO3-+H2O?H3O++CO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、BaSO4的沉淀溶解平衡表达式:BaSO4(s)?Ba2+(aq)+SO42-(aq) |
配制250mL 1mol/L 的稀盐酸溶液,需要12mol/L的浓盐酸的体积为( )
| A、12 mL |
| B、25 mL |
| C、21 mL |
| D、12.5 mL |
在下列物质分类中,前者包含后者的是( )
| A、氧化物、化合物 |
| B、化学反应、复分解反应 |
| C、溶液、胶体 |
| D、溶液、分散系 |
用NA 表示阿伏加德罗常数,下列说法正确的是( )
| A、在常温常压下,11.2L氯气含有的分子数为0.5NA . |
| B、标准状况下,2.24L H2O 含有的分子数等于0.1NA . |
| C、1mol H2 与1mol Cl2 反应生成NA 个HCl |
| D、标准状况下,22.4LN2 和O2混合气体中所含有原子数为2NA |