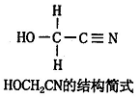
题目内容
18.写出下列物质的电子式:(1)Na2O2

(2)CO2
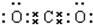
(3)NH4Cl

(4)NH3
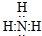 .
.
分析 (1)过氧化钠中两个钠离子与过氧根离子通过离子键结合,两个氧原子通过共用1对电子结合;
(2)二氧化碳中存在两个碳氧双键,C、O原子最外层都达到最外层8个电子;
(3)氯化铵为离子化合物,复杂阳离子和阴离子均需要括号;
(4)氨气中存在3个氮氢键,氮原子最外层8个电子.
解答 解:(1)Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为 ;
;
故答案为: ;
;
(2)二氧化碳中存在两个C=O,二氧化碳的电子式为: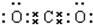 ;
;
故答案为: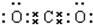 ;
;
(3)氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ;
;
故答案为: ;
;
(4)氨气中存在3个氮氢键,氮原子最外层8个电子,氨气的电子式为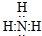 ;
;
故答案为: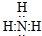 .
.
点评 本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及正确的表示方法,明确离子化合物中阴离子需要标出最外层电子,阳离子直接用离子符号表示.

练习册系列答案
相关题目
8.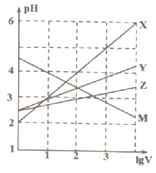 常温下取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3.且HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是( )
常温下取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3.且HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是( )
 常温下取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3.且HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是( )
常温下取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3.且HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是( )| A. | X是HA,M是HB | |
| B. | 常温下pH:NaA溶液>NaB溶液 | |
| C. | 对于$\frac{c({R}^{-})}{c(HR)c(O{H}^{-})}$的值(R代表A或B),一定存在HA>HB | |
| D. | 若常温下浓度均为0.1mol/L的NaA和HA的混合溶液的pH>7,则c(A-)>c(HA) |
6.下列溶液肯定显酸性的是( )
| A. | 含H+的溶液 | B. | 能使酚酞显无色的溶液 | ||
| C. | pH<7的溶液 | D. | C(H+)>C(OH-)的溶液 |
13.同温同压下,等物质的量的SO2和CO2相比较,下列叙述正确的是( )
| A. | 质量比为11:16 | B. | 密度比为11:16 | C. | 体积比为11:16 | D. | 分子个数比为1:1 |
 .
.