题目内容
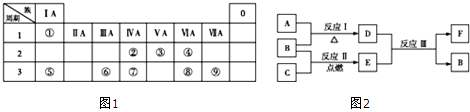
图1为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)已知由①、③、④三种元素组成的某种常见化合物的水溶液呈酸性,则符合该条件的化合物的化学式可能为 (至少写两种).
(2)由表中①、④两种元素按原子个数比为1:1构成的化合物的稀溶液易被催化分解,通常使用的催化剂为 (填序号).
a.MnO2 b.FeCl3 c、Na2SO3 d、KMnO4
(3)图2中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,转化关系如下:
Ⅰ.若B为黄色固体,A为原子半径最小的原子组成的单质.
①F的电子式为 .
②实验测得起始参加反应的B和最后生成的B质量相等,则起始参加反应的A和C的物质的量之比是 .
Ⅱ.若D为淡黄色固体,焰色反应为黄色,组成C的元素的原子最外层电子数是内层电子数的2倍.
①下列关于D的说法正确的是 (填字母).
a.能与水发生化合反应
b.既有氧化性,又有还原性
c.既含离子键,又含非极性共价键
d.是一种碱性氧化物
②用惰性电极将F的饱和溶液进行电解,则阳极反应式是 .

(1)已知由①、③、④三种元素组成的某种常见化合物的水溶液呈酸性,则符合该条件的化合物的化学式可能为
(2)由表中①、④两种元素按原子个数比为1:1构成的化合物的稀溶液易被催化分解,通常使用的催化剂为
a.MnO2 b.FeCl3 c、Na2SO3 d、KMnO4
(3)图2中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,转化关系如下:
Ⅰ.若B为黄色固体,A为原子半径最小的原子组成的单质.
①F的电子式为
②实验测得起始参加反应的B和最后生成的B质量相等,则起始参加反应的A和C的物质的量之比是
Ⅱ.若D为淡黄色固体,焰色反应为黄色,组成C的元素的原子最外层电子数是内层电子数的2倍.
①下列关于D的说法正确的是
a.能与水发生化合反应
b.既有氧化性,又有还原性
c.既含离子键,又含非极性共价键
d.是一种碱性氧化物
②用惰性电极将F的饱和溶液进行电解,则阳极反应式是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置,可知①为H、②为C、③为N、④为O、⑤为Na、⑥为Al、⑦为Si、⑧为S、⑨为Cl.
(1)由①、③、④三种元素组成的硝酸、硝酸铵等水溶液呈酸性;
(2)由表中①、④两种元素按原子个数比为1:1构成的化合物为H2O2,双氧水具有强氧化性,可以氧化亚硫酸钠,过氧化氢含有还原性,可以被高锰酸钾氧化为氧气,在二氧化锰、氯化铁作催化剂条件下,分解生成水与氧气;
(3)图2中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,
Ⅰ.若B为黄色固体,则B为硫,A为原子半径最小的原子组成的单质,则A为H2,可推知D为H2S,硫在C中燃烧生成E,而E与硫化氢反应生成硫与F,可推知C为O2、E为SO2、F为H2O;
Ⅱ.若D为淡黄色固体,焰色反应为黄色,则D为Na2O2,A、B分别为Na、O2中的一种,组成C的元素的原子最外层电子数是内层电子数的2倍,则C原子只能有2个电子层,最外层电子数为4,故C为碳,结合转化关系,可知A为Na,B为O2,E为CO2,F为Na2CO3.
(1)由①、③、④三种元素组成的硝酸、硝酸铵等水溶液呈酸性;
(2)由表中①、④两种元素按原子个数比为1:1构成的化合物为H2O2,双氧水具有强氧化性,可以氧化亚硫酸钠,过氧化氢含有还原性,可以被高锰酸钾氧化为氧气,在二氧化锰、氯化铁作催化剂条件下,分解生成水与氧气;
(3)图2中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,
Ⅰ.若B为黄色固体,则B为硫,A为原子半径最小的原子组成的单质,则A为H2,可推知D为H2S,硫在C中燃烧生成E,而E与硫化氢反应生成硫与F,可推知C为O2、E为SO2、F为H2O;
Ⅱ.若D为淡黄色固体,焰色反应为黄色,则D为Na2O2,A、B分别为Na、O2中的一种,组成C的元素的原子最外层电子数是内层电子数的2倍,则C原子只能有2个电子层,最外层电子数为4,故C为碳,结合转化关系,可知A为Na,B为O2,E为CO2,F为Na2CO3.
解答:
解:由元素在周期表中的位置,可知①为H、②为C、③为N、④为O、⑤为Na、⑥为Al、⑦为Si、⑧为S、⑨为Cl.
(1)由①、③、④三种元素组成的HNO3、NH4NO3等水溶液呈酸性,故答案为:HNO3、NH4NO3;
(2)由表中①、④两种元素按原子个数比为1:1构成的化合物为H2O2,双氧水具有强氧化性,可以氧化亚硫酸钠,过氧化氢含有还原性,可以被高锰酸钾氧化为氧气,在二氧化锰、氯化铁作催化剂条件下,分解生成水与氧气,故选:ab;
(3)图2中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,
Ⅰ.若B为黄色固体,则B为硫,A为原子半径最小的原子组成的单质,则A为H2,可推知D为H2S,硫在C中燃烧生成E,而E与硫化氢反应生成硫与F,可推知C为O2、E为SO2、F为H2O,则:
①F为H2O,其电子式为: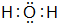 ,故答案为:
,故答案为: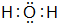 ;
;
②实验测得起始参加反应的硫和最后生成的硫质量相等,生成硫的反应为:2H2S+SO2=3S↓+2H2O,整个过程中氧气获得电子数等于氢气失去电子数,故2n(H2)=4n(O2),则氢气与氧气的物质的量之比为2:1,故答案为:2:1;
Ⅱ.若D为淡黄色固体,焰色反应为黄色,则D为Na2O2,A、B分别为Na、O2中的一种,组成C的元素的原子最外层电子数是内层电子数的2倍,则C原子只能有2个电子层,最外层电子数为4,故C为碳,结合转化关系,可知A为Na,B为O2,E为CO2,F为Na2CO3,则:
①D为Na2O2,
a.过氧化钠能与水反应生成氢氧化钠与氧气,不是化合反应,故a错误;
b.过氧化钠中O元素为-1价,故过氧化钠既有氧化性又有还原性,故b正确;
c.过氧化钠由钠离子与过氧根离子构成,过氧根离子中氧原子之间形成非极性键,故过氧化钠既含离子键又含非极性共价键,故c正确;
d.过氧化钠能与水反应生成氢氧化钠与氧气,故过氧化钠不是碱性氧化物,故d错误,
故答案为:bc;
②用惰性电极将Na2CO3的饱和溶液进行电解,实质是电解水,阳极上发生氧化反应,氢氧根离子在阳极放电生成水与氧气,阳极反应式是:4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑.
(1)由①、③、④三种元素组成的HNO3、NH4NO3等水溶液呈酸性,故答案为:HNO3、NH4NO3;
(2)由表中①、④两种元素按原子个数比为1:1构成的化合物为H2O2,双氧水具有强氧化性,可以氧化亚硫酸钠,过氧化氢含有还原性,可以被高锰酸钾氧化为氧气,在二氧化锰、氯化铁作催化剂条件下,分解生成水与氧气,故选:ab;
(3)图2中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,
Ⅰ.若B为黄色固体,则B为硫,A为原子半径最小的原子组成的单质,则A为H2,可推知D为H2S,硫在C中燃烧生成E,而E与硫化氢反应生成硫与F,可推知C为O2、E为SO2、F为H2O,则:
①F为H2O,其电子式为:
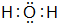 ,故答案为:
,故答案为: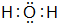 ;
;②实验测得起始参加反应的硫和最后生成的硫质量相等,生成硫的反应为:2H2S+SO2=3S↓+2H2O,整个过程中氧气获得电子数等于氢气失去电子数,故2n(H2)=4n(O2),则氢气与氧气的物质的量之比为2:1,故答案为:2:1;
Ⅱ.若D为淡黄色固体,焰色反应为黄色,则D为Na2O2,A、B分别为Na、O2中的一种,组成C的元素的原子最外层电子数是内层电子数的2倍,则C原子只能有2个电子层,最外层电子数为4,故C为碳,结合转化关系,可知A为Na,B为O2,E为CO2,F为Na2CO3,则:
①D为Na2O2,
a.过氧化钠能与水反应生成氢氧化钠与氧气,不是化合反应,故a错误;
b.过氧化钠中O元素为-1价,故过氧化钠既有氧化性又有还原性,故b正确;
c.过氧化钠由钠离子与过氧根离子构成,过氧根离子中氧原子之间形成非极性键,故过氧化钠既含离子键又含非极性共价键,故c正确;
d.过氧化钠能与水反应生成氢氧化钠与氧气,故过氧化钠不是碱性氧化物,故d错误,
故答案为:bc;
②用惰性电极将Na2CO3的饱和溶液进行电解,实质是电解水,阳极上发生氧化反应,氢氧根离子在阳极放电生成水与氧气,阳极反应式是:4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑.
点评:本题考查元素周期表、元素化合物推断,(3)中物质的颜色是推断突破口,掌握元素化合物的性质是关键,注意对基础知识的全面掌握,难度中等.

练习册系列答案
相关题目
下列金属防腐的措施中,使用牺牲阳极的阴极保护法的是( )
| A、汽车底盘喷涂高分子膜 |
| B、金属护拦表面涂漆 |
| C、将铁制成不锈钢 |
| D、地下钢管连接镁块 |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、常温下,1mol水中约含有10-7 NA个H+ |
| B、25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| C、常温下,100mL 1mol?L-1Na2CO3溶液中阴离子总数大于0.1NA |
| D、常温下1L1mol/LNH4Cl与2L0.5mol/L NH4Cl溶液中,NH4+物质的量相等且都小于1NA |
 如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.回答下列问题:
如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.回答下列问题: