题目内容
2.下列关于有机化合物的说法正确的是( )| A. | 氯乙烯和溴乙烷均能发生加成反应 | |
| B. | 花生油和玉米油都是可皂化的饱和酯类 | |
| C. | 天然气和水煤气的主要成分都是烃类 | |
| D. | 分子式为C10H14的单取代芳烃,其可能的结构有4种 |
分析 A.含有不饱和键的有机物,一般可发生加成反应;
B.植物油多为不饱和酯类;
C.水煤气的主要成分为CO、氢气;
D.分子中含有一个苯环,侧链是烷基,为-C4H9,书写-C4H9的异构体,确定符合条件的同分异构体数目.
解答 解:A.溴乙烷不能发生加成反应,故A错误;
B.植物油多为不饱和酯类,故B错误;
C.水煤气的主要成分为CO、氢气,不属于烃类,故C错误;
D.分子中含有一个苯环,侧链是烷基,为-C4H9,-C4H9的异构体有:-CH2CH2CH2CH3、-CH(CH3)CH2CH3、-CH2CH(CH3)2、-C(CH3)3,故符合条件的结构有4种,故D正确.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的结构和官能团的性质,易错点为D,注意同分异构体的判断,难度中等.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
12. 我国利用合成气直接制烯烃获重大突破,其原理是( )
我国利用合成气直接制烯烃获重大突破,其原理是( )
反应①:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1
反应②:C(s)+H2O(g)?CO(g)+H2(g)△H2
反应③:CO(g)+2H2(g)?CH3OH(g)△H3=-90.1kJ•mol-1
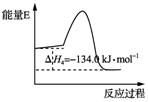
反应④:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H4,能量变化如图所示
反应⑤:3CH3OH(g)?CH3CH═CH2(g)+3H2O(g)△H5=-31.0kJ•mol-1
下列说法正确的是( )
 我国利用合成气直接制烯烃获重大突破,其原理是( )
我国利用合成气直接制烯烃获重大突破,其原理是( )反应①:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1
反应②:C(s)+H2O(g)?CO(g)+H2(g)△H2
反应③:CO(g)+2H2(g)?CH3OH(g)△H3=-90.1kJ•mol-1
反应④:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H4,能量变化如图所示
反应⑤:3CH3OH(g)?CH3CH═CH2(g)+3H2O(g)△H5=-31.0kJ•mol-1
下列说法正确的是( )
| A. | 反应③使用催化剂,△H3减小 | |
| B. | 反应④中正反应的活化能大于逆反应的活化能 | |
| C. | △H1-△H2<0 | |
| D. | 3CO(g)+6H2(g)?CH3CH═CH2(g)+3H2O(g)△H=-121.1 kJ•mol-1 |
13.下列有关物质的性质或应用的说法正确的是( )
| A. | 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于侧链与苯环的相互影响,使侧链和苯环均易被氧化 | |
| B. | 用核磁共振氢谱鉴别1-丙醇和2-丙醇 | |
| C. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 | |
| D. | 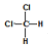 和 和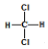 、 、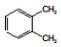 和 和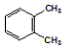 属于同分异构体 属于同分异构体 |
10. 如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )
如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )
 如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )
如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )| A. | 通入H2的电极为负极,A为NH4Cl | |
| B. | 每转移0.1mol电子,消耗1.12L H2 | |
| C. | 溶液中H+向通入N2的一极移动,Cl-向通入H2的一极移动 | |
| D. | 通入N2的电极发生的电极反应式为N2+6e-+8H+═2NH4+ |
2.在实验室模拟工业生产碳酸钠:一定温度下,往一定量饱和NaCl溶液中通入氨气达到饱和后,再不断通入CO2,一段时间后,出现沉淀,过滤得到NaHCO3晶体.
(1)该过程的化学方程式:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.
(2)加热NaHCO3得到纯碱制品,实验室可进行此操作的装置是BC.

(3)得到的纯碱制品含有少量NaHCO3和NaCl,设计实验验证样品中各种组分.试剂和仪器限选用:试管、胶头滴管、过滤装置、Ba(NO3)2溶液、NaOH溶液、AgNO3溶液、澄清石灰水、稀硫酸、稀盐酸、稀硝酸.
(4)某同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,设计了如下实验方案,其中不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是C
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体.
若按A方案进行实验,则原混合物中NaHCO3的质量分数为$\frac{a-\frac{84b}{31}}{a}$(用含a、b的代数式表示)
(1)该过程的化学方程式:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.
(2)加热NaHCO3得到纯碱制品,实验室可进行此操作的装置是BC.

(3)得到的纯碱制品含有少量NaHCO3和NaCl,设计实验验证样品中各种组分.试剂和仪器限选用:试管、胶头滴管、过滤装置、Ba(NO3)2溶液、NaOH溶液、AgNO3溶液、澄清石灰水、稀硫酸、稀盐酸、稀硝酸.
| 步骤一:取少量制品于试管中,加少量蒸馏水,振荡,溶解.往试管中加入过量的Ba(NO3)2溶液振荡,观察 | 现象:溶液中产生大量白色沉淀; 结论:试样中含有Na2CO3. |
| 步骤二:将步骤一的浊液过滤,取滤液于试管中B中,加入适量的NaOH溶液,振荡,观察 | 现象:有少量白色沉淀生成; 结论:样品中含有NaHCO3. |
| 步骤三:将步骤二的浊液过滤,取滤液于试管C中,先加入足量的稀硝酸,再加入少许AgNO3溶液振荡,观察 | 现象:有少量白色沉淀生成; 结论:试样中含有NaCl. |
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体.
若按A方案进行实验,则原混合物中NaHCO3的质量分数为$\frac{a-\frac{84b}{31}}{a}$(用含a、b的代数式表示)
9.水溶液是中学化学的重点研究对象.
(1)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.①浓度为1.0×10-3 mol•L-1的氨水b L;②c(OH-)=1.0×10-3 mol•L-1的氨水c L;③c(OH-)=1.0×10-3 mol•L-1的氢氧化钡溶液d L.
则a、b、c、d之间的关系是b>a=d>c.
(2)已知:Ksp(AgCl)=1.8×10-10,向50mL 0.018mol•L-1的AgNO3溶液中加入相同体积0.020mol•L-1的盐酸,则①c(Ag+)=1.8×10-7mol/L,②此时所得混合溶液的pH=2.
(3)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如表:
①上述盐溶液中的阴离子,结合质子能力最强的是CO32-.
②根据表中数据,浓度均为0.01mol•L-1的下列五种物质的溶液中,分别稀释100倍,pH变化最小的是C(填编号).
A、HCN B、HClO C、HX D、CH3COOH E、H2CO3
③据上表数据,请你判断下列反应不能成立的是BD(填编号).
A.2CH3COOH+Na2CO3═CO2+H2O+2CH3COONa
B.HClO+HCO3-═ClO-+CO2+H2O
C.CH3COOH+NaCN═CH3COONa+HCN
D.CO2+H2O+2NaX═Na2CO3+2HX
(4)将NaHCO3溶液与FeCl3溶液混合,反应的离子方程式是:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑.
(1)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.①浓度为1.0×10-3 mol•L-1的氨水b L;②c(OH-)=1.0×10-3 mol•L-1的氨水c L;③c(OH-)=1.0×10-3 mol•L-1的氢氧化钡溶液d L.
则a、b、c、d之间的关系是b>a=d>c.
(2)已知:Ksp(AgCl)=1.8×10-10,向50mL 0.018mol•L-1的AgNO3溶液中加入相同体积0.020mol•L-1的盐酸,则①c(Ag+)=1.8×10-7mol/L,②此时所得混合溶液的pH=2.
(3)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | NaX |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
②根据表中数据,浓度均为0.01mol•L-1的下列五种物质的溶液中,分别稀释100倍,pH变化最小的是C(填编号).
A、HCN B、HClO C、HX D、CH3COOH E、H2CO3
③据上表数据,请你判断下列反应不能成立的是BD(填编号).
A.2CH3COOH+Na2CO3═CO2+H2O+2CH3COONa
B.HClO+HCO3-═ClO-+CO2+H2O
C.CH3COOH+NaCN═CH3COONa+HCN
D.CO2+H2O+2NaX═Na2CO3+2HX
(4)将NaHCO3溶液与FeCl3溶液混合,反应的离子方程式是:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑.
6.二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3、浓H2SO4反应生成SeO2以回收Se.在回收过程当中涉及到如下两个化学反应
①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;
②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O
下列有关叙述正确的是( )
①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;
②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O
下列有关叙述正确的是( )
| A. | SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2 | |
| B. | ①中Se是氧化产物,I2是还原产物 | |
| C. | 反应①中KI是氧化剂,SeO2是还原剂 | |
| D. | 反应①中每有1.0mol I2生成,转移电子数目为4NA |