题目内容
8.下列各组微粒具有相同的质子数和电子数的是( )| A. | OH-、H2O | B. | NH3、NH4+ | C. | H3O+、NH2- | D. | HC1、H2S |
分析 根据原子的质子数相加即为微粒的质子数,阴离子中电子数=质子数+电荷数,阳离子中电子数=质子数-电荷数来分析解答.
解答 解:A、OH-、H2O的质子数分别为9、10,电子数分别为10、10,故A错误;
B、NH3、NH4+的质子数都是10、11,电子数都是10,故B错误
C、H3O+、NH2-的质子数分别为11,9、电子数分别为10,10,故C错误;
D、HC1、H2S的质子数都是18、18,电子数都是18,故D正确;
故选D.
点评 本题考查微粒的质子数和电子数,明确质子数和电子数的计算及中性微粒中质子数等于电子数是解答本题的关键.

练习册系列答案
相关题目
18.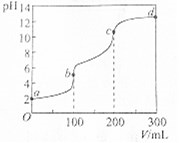 室温下,向100mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol•L-1 NaOH溶液的pH随NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )
室温下,向100mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol•L-1 NaOH溶液的pH随NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )
 室温下,向100mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol•L-1 NaOH溶液的pH随NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )
室温下,向100mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol•L-1 NaOH溶液的pH随NaOH溶液体积的变化曲线如图所示.下列有关说法正确的是( )| A. | a点溶液的pH=2,草酸溶液的浓度为0.005mol•L-1 | |
| B. | b点对应溶液中:c(Na+)>c(HC2O4-)>c(OH-)>c(C2O42-) | |
| C. | b→c段,反应的离子方程式为HC2O4-+OH-═C2O42-+H2O | |
| D. | c→d段,溶液中C2O42-的水解程度逐渐增强 |
19.直链烷烃的通式可用CnH2n+2表示,现有一系列芳香烃,按下列特点排列: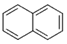 ,
,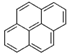 ,
,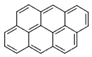 ,…若用分子式表示这一系列化合物,其第十五项应为( )
,…若用分子式表示这一系列化合物,其第十五项应为( )
 ,
, ,
, ,…若用分子式表示这一系列化合物,其第十五项应为( )
,…若用分子式表示这一系列化合物,其第十五项应为( )| A. | C15H24 | B. | C94H36 | C. | C60H36 | D. | C34H96 |
16.下列说法中,正确的是( )
| A. | 在离子化合物中不可能含有共价键 | |
| B. | 在共价化合物中也可能含有离子键 | |
| C. | 凡含有离子键的化合物一定是离子化合物 | |
| D. | 完全由非金属元素组成的化合物一定是离子化合物 |
3.在如图所示的微粒中,结合电子能力最强的是( )
| A. | 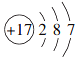 | B. | 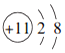 | C. |  | D. |  |
20.下列说法正确的是( )
| A. | 金属与非金属元素形成的化合物一定是离子化合物 | |
| B. | 干冰气化过程中只需克服分子间作用力 | |
| C. | HF的热稳定性很好,是因为HF分子间存在氢键 | |
| D. | 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构 |
17.下列有关有机物的说法不正确的是( )
| 选项 | 项目 | 分析 |
| A | 制备乙烯、制备硝基苯 | 实验时均用到了温度计 |
| B | 乙烯制备乙醇、氯乙烷制备乙醇 | 属于同一反应类型 |
| C | 丙烯可以使溴水和酸性高锰酸钾溶液褪色 | 褪色原理不同 |
| D | 乙醇燃烧、乙醇使重铬酸钾变色 | 均为氧化反应 |
| A. | A | B. | B | C. | C | D. | D |
18.双酚A作为食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大.下列有关双酚A的叙述不正确的是( )
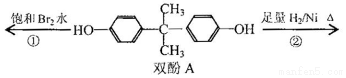

| A. | 双酚A的分子式是C15H16O2 | |
| B. | 反应①中,1mol双酚A最多消耗2mol Br2 | |
| C. | 反应②的产物中只有一种官能团 | |
| D. | 双酚A的核磁共振氢谱显示氢原子数之比是1:2:2:3 |
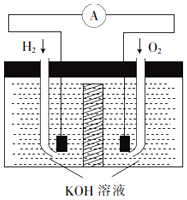 氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.
氢氧燃料电池是符合绿色化学理念的新型发电装置.其工作原理如图所示,该电池的电极表面镀了一层细小的铂粉,已知铂吸附气体的能力强,且性质稳定.