题目内容
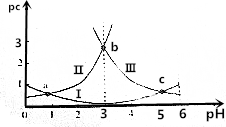
10.pH是溶液中c(H+)的负对数,若定义pc是溶液中溶质物质的量浓度的负对数,则常温下,某浓度的草酸(H2C2O4)水溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)随着溶液pH的变化曲线如图所示:已知草酸的电离常数K${\;}_{{a}_{1}}$=5.6×10-2,K${\;}_{{a}_{2}}$=5.4×10-5
下列叙述正确的是( )
| A. | 曲线Ⅰ表示H2C2O4的变化 | |
| B. | pH=4时,c(HC2O4-)>c(C2O42-) | |
| C. | c(H2C2O4)+c(HC2O4-)+c(C2O42-)在a点和b点一定相等 | |
| D. | 常温下,$\frac{c({H}_{2}{C}_{2}{O}_{4})•c({C}_{2}{{O}_{4}}^{2-})}{{c}^{2}(H{C}_{2}{{O}_{4}}^{-})}$随pH的升高先增大后减小 |
分析 H2C2O4?H++HC2O4-,HC2O4-?H++C2O42-,pH增加促进电离平衡正向移动,所以由图可知:曲线Ⅰ是HC2O4-的物质的量浓度的负对数,曲线Ⅱ是H2C2O4的物质的量浓度的负对数,曲线Ⅲ是C2O42-的物质的量浓度的负对数,由此分析解答.
解答 解:A、曲线Ⅰ表示HC2O4-的物质的量浓度的负对数的变化,而不是H2C2O4的变化,故A错误;
B、pH=4时,pc(C2O42-)>pc(HC2O4-),所以c(HC2O4-)>c(C2O42-),故B正确;
C、根据物料守恒,c(H2C2O4)+c(HC2O4-)+c(C2O42-)在a点和b点一定相等,故C正确;
D、常温下,$\frac{c({H}_{2}{C}_{2}{O}_{4})•c({C}_{2}{{O}_{4}}^{2-})}{{c}^{2}(H{C}_{2}{{O}_{4}}^{-})}$的分子和分母同乘以氢离子的浓度,即为$\frac{{K}_{a2}}{{K}_{a1}}$,只要温度不变,比值不变,故D错误;
故选BC.
点评 本题考查酸碱混合物的定性判断和计算,侧重于学生的分析能力和计算能力的考查,注意把握图象的含义,C选项为易错点,注意对平衡常数的理解与灵活运用.

练习册系列答案
相关题目
20.已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数c>d | B. | 非金属性Y<Z | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 原子半径W>X |
1.单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法不正确的是( )


| A. | 单斜硫和正交硫互为同素异形体 | |
| B. | 单斜硫比正交硫稳定 | |
| C. | 两种硫的燃烧反应均为放热反应 | |
| D. | S(s,单斜)=S(s,正交)△H=-0.33 kJ•mol-1 |
19.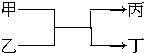 若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
 若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )| A. | 碳和镁 | B. | 氟气和氧气 | C. | 碳和氢气 | D. | 氧气和硫 |
20.下列有关有机化合物的说法正确的是( )
| A. | 丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 | |
| B. | 乙烯和苯使溴水褪色的原理相同 | |
| C. | 乙醇和乙酸均可与钠反应放出氢气 | |
| D. | 糖类、油脂、蛋白质均为高分子化合物 |

 ;
;