题目内容
金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,装置A的作用是制取氯气,虚线框内是除杂装置,请回答下列问题:
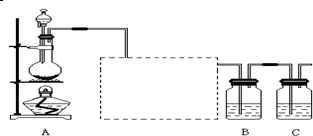
(1)装置A的分液漏斗中盛装的试剂是 ,烧瓶中加入的试剂是 .
(2)画出虚线框内的实验装置图,并注明所加试剂 .
(3)装置B中盛放的试剂是 (选填下列所给试剂的代码),实验现象为 ,化学反应方程式是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)装置C中盛放烧碱溶液,目的是 .

(1)装置A的分液漏斗中盛装的试剂是
(2)画出虚线框内的实验装置图,并注明所加试剂
(3)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)装置C中盛放烧碱溶液,目的是
考点:实验装置综合,非金属在元素周期表中的位置及其性质递变的规律
专题:实验设计题
分析:(1)从实验室制取氯气的原理分析;
(2)氯气在饱和食盐水中溶解度很小,HCl易溶于水;
(3)从置换反应判断元素非金属性强弱分析,氯气能把硫元素从其硫化钠溶液中置换出来;
(4)氯气为有毒气体,要进行尾气处理.
(2)氯气在饱和食盐水中溶解度很小,HCl易溶于水;
(3)从置换反应判断元素非金属性强弱分析,氯气能把硫元素从其硫化钠溶液中置换出来;
(4)氯气为有毒气体,要进行尾气处理.
解答:
解:(1)为验证氯元素的非金属性比硫元素的非金属性强,需要用氯气置换出硫,则必须用装置A制备氯气,实验室通常用浓盐酸与二氧化锰反应制取氯气,则A装置中A的分液漏斗中盛装的试剂是浓盐酸,烧瓶中加入的试剂是MnO2;
故答案为:浓盐酸;MnO2;
(2)由于用浓盐酸制取氯气,且需要加热,即实验过程中要挥发出HCl气体,因此虚线框部分应是除去HCl气体的装置,可以使用洗气瓶,瓶内盛装饱和食盐水,既除去HCl,又降低氯气在水中的溶解度,所用装置为: ;
;
故答案为: ;
;
(3)要在B中发生氯气置换出硫的反应,在给定试剂中只能选取Na2S溶液,发生的是置换反应,化学方程式为:Na2S+Cl2=2NaCl+S↓;
故答案为:A;有淡黄色沉淀生成;Na2S+Cl2=2NaCl+S↓;
(4)氯气为有毒气体,要进行尾气处理,氯气能与氢氧化钠溶液反应,所以装置C中盛放烧碱溶液的作用是吸收氯气,防止污染大气;
故答案为:吸收氯气,防止污染大气.
故答案为:浓盐酸;MnO2;
(2)由于用浓盐酸制取氯气,且需要加热,即实验过程中要挥发出HCl气体,因此虚线框部分应是除去HCl气体的装置,可以使用洗气瓶,瓶内盛装饱和食盐水,既除去HCl,又降低氯气在水中的溶解度,所用装置为:
 ;
;故答案为:
 ;
;(3)要在B中发生氯气置换出硫的反应,在给定试剂中只能选取Na2S溶液,发生的是置换反应,化学方程式为:Na2S+Cl2=2NaCl+S↓;
故答案为:A;有淡黄色沉淀生成;Na2S+Cl2=2NaCl+S↓;
(4)氯气为有毒气体,要进行尾气处理,氯气能与氢氧化钠溶液反应,所以装置C中盛放烧碱溶液的作用是吸收氯气,防止污染大气;
故答案为:吸收氯气,防止污染大气.
点评:本题以实验题的形式考查了比较Cl和S的非金属性强弱的方法,注意从整体的角度把握题目需要解答的问题,题目难度不大,掌握常见非金属元素的性质是关键.

练习册系列答案
相关题目
同温同压下,在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体.两容器内的气体一定具有相同的( )
| A、原子数 | B、密度 |
| C、质量 | D、分子数 |
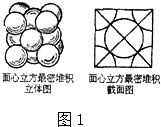 (1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是
(1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是