题目内容
8.写出下列物质在水溶液中的电离方程式FeCl3:FeCl3=Fe3++3Cl-(NH4)2CO3:(NH4)2CO3=2NH4++CO32-,Ba(OH)2:Ba(OH)2=Ba2++2OH- NaHSO4:NaHSO4=Na++H++SO42-.
分析 强电解质完全电离,用等号;弱电解质,部分电离,用可逆号;原子团不能拆.
解答 解:氯化铁为强电解质,完全电离,电离方程式:FeCl3=Fe3++3Cl-,
故答案为:FeCl3=Fe3++3Cl-;
碳酸铵为强电解质,完全电离,电离方程式:(NH4)2CO3=2NH4++CO32-;
故答案为:(NH4)2CO3=2NH4++CO32-;
氢氧化钡为强电解质,完全电离,电离方程式:Ba(OH)2=Ba2++2OH-,
故答案为:Ba(OH)2=Ba2++2OH-;
硫酸氢钠为强电解质,完全电离,电离方程式:NaHSO4=Na++H++SO42-;
故答案为:NaHSO4=Na++H++SO42-.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列各选项中所述的两个量,前者一定大于后者的是( )
| A. | 相同条件下,H2分别与F2、Cl2反应的反应速率 | |
| B. | 纯水在80℃和25℃时的pH | |
| C. | 在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数 | |
| D. | 1 L 0.3 mol•L-1 CH3COOH溶液和3 L 0.2 mol•L-1 CH3COOH溶液中的H+数目 |
7.要使含有Ba2+、Al3+、Cu2+、Mg2+、Ag+等离子的溶液中的各离子逐一形成沉淀析出,下列所选择的试剂及加入试剂的顺序正确的是( )
| A. | H2SO4-HCl-H2S-NaOH-CO2 | B. | HCl-H2SO4-Na2S-NaOH-CO2 | ||
| C. | NaCl-Na2SO4-Na2S-NaOH-CH3COOH | D. | Na2S-Na2SO4-NaCl-NaOH-HCl |
4.将下列每组内的四种物质同时加入到水中,充分搅拌后,既有氧化还原反应发生,又有沉淀产生的一组是( )
| A. | Na2O2、NH4Cl、NaCl、Na2SO4 | B. | FeO、AlCl3、Na2SiO3、硝酸 | ||
| C. | KHCO3、Ca(OH)2、MgCl2、硫酸 | D. | NaCO3、BaCl2、K2S、盐酸 |
3.反应Fe(固)+CO2(气)?FeO(固)+CO(气)的平衡常数为K1;
反应Fe(固)+H2O(气)?FeO(固)+H2(气)的平衡常数为K2.
在不同温度时K1、K2的值如下表:
(1)推导反应CO2(气)+H2(气)?CO(气)+H2O(气)的平衡常数K与K1、K2的关系式:$\frac{{K}_{1}}{{K}_{2}}$.
(2)计算K值:温度为973开时K=0.618;1173开时:K=1.29.通过K值的计算(1)反应是吸热 反应(填“吸热”或“放热”).
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2,在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件.各物质的浓度变化如下表:
①前2min,用CO表示的该化学反应的速率是:0.0013mol/(L.min).
②在3~4min之间,反应处于平衡状态(填“平衡”或“非平衡”).
③第6min时,平衡向正反应方向移动,可能的原因是升高温度或移走水蒸气.
反应Fe(固)+H2O(气)?FeO(固)+H2(气)的平衡常数为K2.
在不同温度时K1、K2的值如下表:
| 温度(绝对温度) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(2)计算K值:温度为973开时K=0.618;1173开时:K=1.29.通过K值的计算(1)反应是吸热 反应(填“吸热”或“放热”).
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2,在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件.各物质的浓度变化如下表:
| 时间/min | CO2 | H2 | CO | H2O |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
②在3~4min之间,反应处于平衡状态(填“平衡”或“非平衡”).
③第6min时,平衡向正反应方向移动,可能的原因是升高温度或移走水蒸气.
20.下列说法不正确的是( )
| A. | 很多食物含有维生素,但蔬菜、水果比其他食物能提供更多的维生素 | |
| B. | 选择食物时,要考虑含营养素的种类、含量及是否易被人体吸收和利用 | |
| C. | 人体每天需要营养素的量是相对稳定的 | |
| D. | 三大热能食物中,糖类提供的热能最多,热值也最大 |
18.下列有关化学用语能确定为丙烯的是( )
| A. | 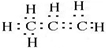 | B. | C3H6 | C. |  | D. |  |
