题目内容
下列说法正确的是( )
| A、向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 |
| B、欲除CO2中少量SO2气体,可将此混合气体通过盛饱和碳酸钠溶液的洗气瓶 |
| C、氯气有漂白性,所以氯气能使有色布条褪色 |
| D、漂白粉的主要成分是CaCl2和Ca(ClO)2,应密封保存 |
考点:氯气的化学性质,氯、溴、碘及其化合物的综合应用,二氧化硫的化学性质
专题:元素及其化合物
分析:A.久置的氯水就是盐酸溶液;
B.二氧化硫和二氧化碳都和碳酸钠反应;
C.氯气没有漂白性,次氯酸有漂白性;
D.漂白粉的主要成分是CaCl2和Ca(ClO)2,有效成分是Ca(ClO)2,但不稳定.
B.二氧化硫和二氧化碳都和碳酸钠反应;
C.氯气没有漂白性,次氯酸有漂白性;
D.漂白粉的主要成分是CaCl2和Ca(ClO)2,有效成分是Ca(ClO)2,但不稳定.
解答:
解:A.次氯酸不稳定易分解生成HCl和氧气,所以久置的氯水就是盐酸溶液,向久置的氯水中滴入紫色石蕊试液,溶液将只变红不褪色,故A错误;
B.二氧化碳和二氧化硫都和碳酸钠反应,但二氧化碳和碳酸氢钠不反应,所以应该用饱和的碳酸氢钠溶液除去二氧化碳中的二氧化硫,故B错误;
C.氯气没有漂白性,次氯酸有漂白性,所以氯气不能使干燥有色布条褪色,故C错误;
D.漂白粉的主要成分是CaCl2和Ca(ClO)2,有效成分是Ca(ClO)2,但不稳定,易和空气中二氧化碳、水反应生成次氯酸而失效,故D正确;
故选D.
B.二氧化碳和二氧化硫都和碳酸钠反应,但二氧化碳和碳酸氢钠不反应,所以应该用饱和的碳酸氢钠溶液除去二氧化碳中的二氧化硫,故B错误;
C.氯气没有漂白性,次氯酸有漂白性,所以氯气不能使干燥有色布条褪色,故C错误;
D.漂白粉的主要成分是CaCl2和Ca(ClO)2,有效成分是Ca(ClO)2,但不稳定,易和空气中二氧化碳、水反应生成次氯酸而失效,故D正确;
故选D.
点评:本题考查除杂、物质的性质等知识点,明确物质的性质即可解答,注意除杂时不能引进新的杂质,注意氯气没有漂白性,为易错点.

练习册系列答案
相关题目
等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出H2最多的是( )
| A、2mol/L H2SO4溶液 |
| B、3mol/L CuSO4溶液 |
| C、6mol/L KOH溶液 |
| D、3mol/L Ba(OH)2溶液 |
下列操作中不正确的是( )
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、过滤操作时,玻璃棒与三层滤纸的一边接触 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、萃取操作时,一般选择有机萃取剂,且萃取剂必须与水不互溶 |
实验是化学研究的基础.下列对实验现象的描述错误的是( )
 |  | 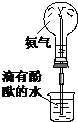 |  |
| ① | ② | ③ | ④ |
| A、实验①中溶液变黄色 |
| B、实验②试管中混合溶液变红色 |
| C、实验③中烧瓶内溶液变红色 |
| D、实验④中出现砖红色沉淀 |
将铁屑溶于过量盐酸后,再加入下列物质:①硫酸②硝酸锌③氯化铜④氯水,产生的Fe3+是( )
| A、①④ | B、②④ | C、只有④ | D、①③ |
下列有关物质与其用途(括号内为其用途)不相对应的是( )
| A、SiO2(制光纤) |
| B、氮化硅陶瓷(制导热剂) |
| C、钢化玻璃(汽车窗玻璃) |
| D、Si和Ge(半导体材料) |
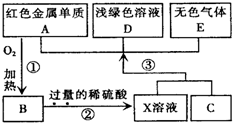 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答: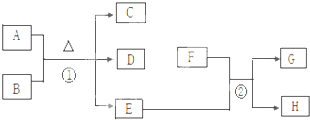 如图中A~H均为中学化学中常见的物质.已知A为紫红色金属,D能使品红溶液褪色,E为生活中常见的无色无味液体,F为黄绿色气体.请回答下列问题:
如图中A~H均为中学化学中常见的物质.已知A为紫红色金属,D能使品红溶液褪色,E为生活中常见的无色无味液体,F为黄绿色气体.请回答下列问题: