题目内容
12.用铜、铬的氧化物作催化剂,HCl制Cl2的原理为:4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 kJ•mol-1,下列说法正确的是( )| A. | 平衡时,将生成的水蒸气除去,有利于提高HCl的转化率 | |
| B. | 在恒容绝热容器中进行时,随着反应的进行,气体的压强一定不断减小 | |
| C. | 恒压容器中,反应到平衡后通入惰性气体,平衡不移动 | |
| D. | 平衡时,其他条件不变,增大催化剂用量,反应的平衡常数将变大 |
分析 A.将生成的水蒸气除去,生成物浓度减小,平衡正向移动;
B.在恒容绝热容器中进行时,该反应为放热反应,体系温度升高;
C.恒压容器中,反应到平衡后通入惰性气体,体积增大,相等于压强减小;
D.催化剂对平衡移动无影响,且K与温度有关.
解答 解:A.将生成的水蒸气除去,生成物浓度减小,平衡正向移动,则有利于提高HCl的转化率,故A正确;
B.在恒容绝热容器中进行时,该反应为放热反应,体系温度升高,气体的体积受温度、压强影响,则气体的压强可能增大,故B错误;
C.恒压容器中,反应到平衡后通入惰性气体,体积增大,相等于压强减小,则平衡正向移动,故C错误;
D.催化剂对平衡移动无影响,则平衡时,其他条件不变,增大催化剂用量,反应的平衡常数不变,故D错误;
故选A.
点评 本题考查化学平衡移动,为高频考点,把握温度、压强、浓度对反应的影响是解答的关键,侧重分析与应用能力的考查,注意选项B中绝热的条件为易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.有四种微粒的结构示意图如图,下列说法错误的是( )
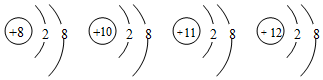
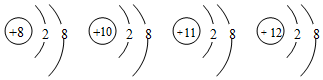
| A. | 它们属于不同种元素 | |
| B. | 它们的核外电子排布相同 | |
| C. | 它们都是离子 | |
| D. | 它们都具有稀有气体原子的稳定结构 |
3.若NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 含lmolH2SO4的浓硫酸与足量铜在加热条件下反应,转移的电子总数为NA | |
| B. | 0.1 L0.5mol/LCH3COOH 溶液中含有的氢离子为0.05NA | |
| C. | 粗铜精炼时阳极质量减少6.4g,则外电路上通过0.2NA电子 | |
| D. | 1molCH3COONa和少量CH3COOH溶于水所得到的中性溶液中,CH3COO-的数目为NA |
20.同位素示踪技术已广泛应用在农业、工业、医学、地质及考古等领域.下列有关叙述正确的是( )
| A. | 14C与12C是两种不同的元素或核素 | |
| B. | 通过化学变化可以实现16O与18O之间的相互转化 | |
| C. | 35Cl2与37Cl2互为同素异形体 | |
| D. | 铯元素的两种同位素中137Cs比133Cs多4个中子 |
7.下列关于离子共存或离子反应的说法正确的是( )
| A. | 某无色溶液中可能大量存在H+、Cl-、MnO4- | |
| B. | pH=2的溶液中可能大量存在Na+、NH4+、SiO32- | |
| C. | 向Ca(HCO3)2溶液中加入少量NaOH溶液的反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | 向稀HNO3中滴加Na2SO3溶液的反应:SO32-+2H+═SO2↑+H2O |
17.近年来,全国安全事故频发,折射出人们对化学品与安全知识的极度缺乏,下列有关化学品与安全的说法或操作错误的是( )
| A. | A.运石油的油罐车上应贴  标志,并由专人押运 标志,并由专人押运 | |
| B. | 不慎将酒精洒到桌面上引起着火,可用水扑灭 | |
| C. | 氢氧化钠浓溶液溅入眼中,应立即用大量水冲洗,再用硼酸稀溶液冲洗 | |
| D. | 右图装置可分离CH3COOC2H5和碳酸钠饱和溶液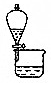 |
16.下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2加热时发生反应
②Fe与过量稀H2SO4反应后,再向其中加KNO3
③Fe与过量的S加热时发生反应
④Fe(NO3)2溶液中加少量盐酸
⑤Fe和Fe2O3的混合物溶于盐酸中.
①过量的Fe与Cl2加热时发生反应
②Fe与过量稀H2SO4反应后,再向其中加KNO3
③Fe与过量的S加热时发生反应
④Fe(NO3)2溶液中加少量盐酸
⑤Fe和Fe2O3的混合物溶于盐酸中.
| A. | ①②③ | B. | ②④⑤ | C. | ①④⑤ | D. | ①②④ |
17.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 2.4 g镁在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.8 NA | |
| B. | 标准状况下,5.6 L二氧化碳气体中含有的氧原子数为0.5 NA | |
| C. | 8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1 NA | |
| D. | 0.1 L 0.5 mol/L CH3COOH溶液中含有的氢离子数为0.05 NA |
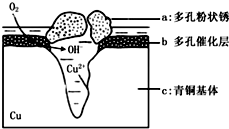 图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.
图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.