题目内容
浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48L(标准状况).试计算:
(1)反应后生成硫酸铜的物质的量.
(2)若将反应后的溶液稀释至500mL,计算该溶液中硫酸铜的物质的量浓度.
(1)反应后生成硫酸铜的物质的量.
(2)若将反应后的溶液稀释至500mL,计算该溶液中硫酸铜的物质的量浓度.
考点:化学方程式的有关计算
专题:计算题
分析:铜和浓硫酸的反应方程式为Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,
(1)根据硫酸铜和二氧化硫的关系式计算硫酸铜的物质的量;
(2)根据稀释前后溶质的物质的量不变计算稀释后硫酸铜的浓度.
| ||
(1)根据硫酸铜和二氧化硫的关系式计算硫酸铜的物质的量;
(2)根据稀释前后溶质的物质的量不变计算稀释后硫酸铜的浓度.
解答:
解:(1)设硫酸铜的物质的量为n,
Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑
1mol 22.4L
n(CuSO4) 4.48L
1mol:22.4L=n(CuSO4):4.48L
n(CuSO4)=
=0.2mol,
答:硫酸铜的物质的量为0.2mol;
(2)溶液稀释前后溶质的物质的量不变,所以c(CuSO4)=
=0.4mol/L,
答:硫酸铜的浓度为0.4mol/L.
Cu+2H2SO4(浓)
| ||
1mol 22.4L
n(CuSO4) 4.48L
1mol:22.4L=n(CuSO4):4.48L
n(CuSO4)=
| 1mol×4.48L |
| 22.4L |
答:硫酸铜的物质的量为0.2mol;
(2)溶液稀释前后溶质的物质的量不变,所以c(CuSO4)=
| 0.2mol |
| 0.5L |
答:硫酸铜的浓度为0.4mol/L.
点评:本题考查了根据方程式进行计算,正确书写方程式是解本题关键,再结合物质之间的关系式进行解答,难度不大.

练习册系列答案
相关题目
X、Y、Z、W、R、Q是6种短周期主族元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R、Q处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法不正确的是( )
| A、同周期元素的离子中W离子半径最小 |
| B、元素X能与元素Y形成共价化合物X2Y2 |
| C、工业上用二氧化锰和浓盐酸制取Q的单质 |
| D、元素Z、W、R的最高价氧化物对应的水化物之间均能反应 |
下列反应的离子方程式书写正确的是( )
| A、钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ |
| B、金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-+H2↑ |
| C、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| D、铜和浓硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
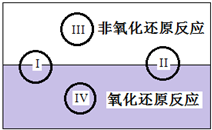 氧化还原反应在生产、生活中具有广泛的用途.
氧化还原反应在生产、生活中具有广泛的用途. 2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.
2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.