题目内容
20.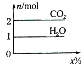 将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )| A | B | C | D | |
| 甲 | 戊烯 | 已烯 | 己二炔(C6H6) | 己烷 |
| 乙 | 环己烷(C6H12) | 苯 | 苯 | 乙醇 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据有机物燃烧生成CO2、H2O的质量与甲气体在混合液中质量分数关系图可知,随有机物甲的含量增大,生成的二氧化碳和水的质量不变,则在混合物中C、H元素的质量分数为定值,以此来解答.
解答 解:有机物燃烧生成CO2、H2O的质量与甲气体在混合液中质量分数关系图可知,随有机物甲的含量增大,生成的二氧化碳和水的质量不变,则在混合物中C、H元素的质量分数为定值,且生成二氧化碳和水的物质的量之比为:2:1,所以有机物分子组成中碳氢的物质的量之比为1:1,则
A、戊烯(C5H10)、环己烷(C6H12)的最简式都是CH2,不符号题意,故A错误;
B、已烯(C6H12)、苯(C6H6)的最简式不同,则在混合物中甲与乙的C、H元素的质量分数不同,不符合题意,故B错误;
C、己二炔(C6H6)、苯(C6H6)的最简式相同同,则在混合物中碳氢的物质的量之比为1:1,符合题意,故C正确;
D、己烷(C6H14)、乙醇(C2H6O)的最简式不同,则在混合物中甲与乙的C、H元素的质量分数不同,不符合题意,故D错误;
故选C.
点评 本题考查有机物燃烧的计算,明确图象中二氧化碳和水的质量不变得出混合物中C、H元素的质量分数为定值是解答本题关键,省略了利用各个方程式计算的繁琐,直接利用有机物的最简式即可确定C、H元素的质量分数,具有一定的技巧性.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
10.向下列各离子组的溶液中通入足量相应气体后,各离子还能大量存在的是( )
| A. | 氯气:Na+、Ba2+、HSO3-、I- | B. | 二氧化碳:Ca2+、NO3-、Ba2+、Cl- | ||
| C. | 氨气:Fe3+、Al3+、Na+、NO3- | D. | 二氧化硫:Ba2+、K+、NO3-、Cl- |
15.图为番茄电池的示意图,下列说法正确的是( )
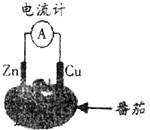

| A. | 电流由锌通过导线流向铜 | B. | 负极反应为Zn-2e-=Zn2+ | ||
| C. | 一段时间后,铜片质量会减少 | D. | 一段时间后,锌片质量会增加 |
5.异戊烷(CH3)2CHCH2CH3的一氯代物与二氯代物的同分异构体数目分别是(不含立体异构)( )
| A. | 4,10 | B. | 5,11 | C. | 4,9 | D. | 4,11 |
9.已知:①lmolH2分子中化学键断裂时需要吸收436kJ的能量②1mol C12分子中化学键断裂时需要吸收243kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431kJ的能量下列叙述中正确的是( )
| A. | 氢气和氯气反应生成氯化氢气体的热化学方程式是:H2(g)+Cl2(g)=2HCl(g) | |
| B. | 氢气和氯气反应生成2mol氯化氢气体,反应的△H=+183KJ•mol-1 | |
| C. | 氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183KJ•mol-1 | |
| D. | 氢气和氯气反应生成1mol氯化氢气体,反应的△H=+183KJ•mol-1 |
17.在100mL某混合溶液中,c(HNO3)=0.4mol/L,c(H2SO4)=0.25mol/L,向其中加入 1.92g铜粉,微热,充分反应后溶液中c(NO3-)约为( )
| A. | 0.15mol/L | B. | 0.20mol/L | C. | 0.225mol/L | D. | 0.30mol/L |
 .
.