题目内容
在298K、100kPa时,已知:2H2O(g)=O2(g)+2H2(g)△H1
Cl2(g)+H2(g)=2HCl(g )△H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
Cl2(g)+H2(g)=2HCl(g )△H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
| A、△H3=△H1+2△H2 |
| B、△H3=△H1+△H2 |
| C、△H3=△H1-2△H2 |
| D、△H3=△H1-△H2 |
考点:用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:设2H2O(g)=O2(g)+2H2(g)△H1 …①
Cl2(g)+H2(g)=2HCl(g )△H2…②
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3…③
由盖斯定律可知,③=①+2×②分析.
Cl2(g)+H2(g)=2HCl(g )△H2…②
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3…③
由盖斯定律可知,③=①+2×②分析.
解答:
解:设2H2O(g)=O2(g)+2H2(g)△H1 …①
Cl2(g)+H2(g)=2HCl(g )△H2…②
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3…③
由盖斯定律可知,③=①+2×②,因此△H3=△H1+2△H2.
故选A.
Cl2(g)+H2(g)=2HCl(g )△H2…②
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3…③
由盖斯定律可知,③=①+2×②,因此△H3=△H1+2△H2.
故选A.
点评:本题考查学生利用盖斯定律来计算反应热的关系,明确化学反应的关系,在加和反应时等号同侧的相加,当乘以一个系数时反应热也要乘以这个系数来解答即可.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
已知:①2C(s)+O2(g)═2CO(g)△H=-221.0kJ?mol-1;
②2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1.
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
②2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1.
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
| A、262.6 kJ?mol-1 |
| B、-131.3 kJ?mol-1 |
| C、-352.3 kJ?mol-1 |
| D、131.3 kJ?mol-1 |
已知:C(s)+
O2(g)═CO(g)△H=-110.5kJ?mol-1①
C(s)+O2(g)═CO2(g)△H=-393.51kJ?mol-1②
计算反应C(s)+CO2(g)═2CO(g)的反应热△H的值为( )
| 1 |
| 2 |
C(s)+O2(g)═CO2(g)△H=-393.51kJ?mol-1②
计算反应C(s)+CO2(g)═2CO(g)的反应热△H的值为( )
| A、-283.01kJ?mol-1 |
| B、+172.51kJ?mol-1 |
| C、+283.1kJ?mol-1 |
| D、+504.00kJ?mol-1 |
已知25℃时一些难溶物质的溶度积常数如下:
根据上表数据,判断下列化学方程式不正确的是( )
| 化学式 | Zn(OH)2 | ZnS | AgCl | Ag2S | MgCO3 | Mg(OH)2 |
| 溶度积 | 5×10-17 | 2.5×10-22 | 1.8×10-10 | 6.3×10-50 | 6.8×10-6 | 1.8×10-11 |
| A、2AgCl+Na2S═2NaCl+Ag2S | ||||
B、MgCO3+H2O
| ||||
| C、ZnS+2H2O═Zn(OH)2+H2S↑ | ||||
| D、Mg(HCO3)2+2Ca(OH)2═Mg(OH)2↓+2CaCO3↓+2H2O |
 某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题.
某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题.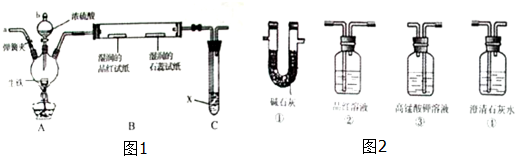
 ,不符合
,不符合