题目内容
7.下列说法错误的是( )| A. | 1mol白磷分子晶体中,含有的共价键为6mol | |
| B. | 离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键未被破坏 | |
| C. | 在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl- (或Na+) | |
| D. | 由于氢键作用,HF是一种非常稳定的化合物 |
分析 A、白磷是4个原子的正四面体;
B、分子晶体在熔化时破坏分子间作用力;
C、氯化钠晶体中钠离子或氯离子的配位数都是6;
D、氢键是影响物质的物理性质.
解答 解:A、白磷是4个原子的正四面体,分子中含有6个P-P键,所以1mol白磷分子晶体中,含有的共价键为6mol,故A正确;
B、离子晶体是通过离子键将阴、阳离子结合在一起的,所以熔化时,离子键被破坏,分子晶体是通过范德华力结合时,熔化时化学键不受影响,故B正确;
C、氯化钠晶体中钠离子或氯离子的配位数都是6,所以在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl-(或Na+),故C正确;
D、氢键是影响物质的物理性质,而稳定性是化学性质,故D错误;
故选D.
点评 本题考查微粒之间的相互作用,明确物质构成白磷的结构及微粒之间作用力是解本题关键,易错选项是D,注意氢键是影响物质的物理性质,为易错点.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
17.胶体区别于其它分散系最本质的特征是( )
| A. | 外观澄清、稳定 | B. | 分散质粒子直径为1---100nm | ||
| C. | 分散至粒子能透过半透膜 | D. | 丁达尔现象 |
18.在25℃时,某稀溶液中由水电离产生的c(OH-)=10-10 mol•L-1.下列有关该溶液的叙述正确的是( )
| A. | 该溶液一定呈酸性 | |
| B. | 该溶液中c(H+)可能等于10-5 mol•L-1 | |
| C. | 该溶液的pH可能为4也可能为10 | |
| D. | 该溶液有可能呈中性 |
15.有两个无标签的试剂瓶,分别盛有固体K2CO3、NaHCO3,有四位同学为鉴别它们采用了以下不同方法,其中不可行的是( )
| A. | 分别将它们配制成溶液,再加入澄清石灰水,观察是否有沉淀产生 | |
| B. | 分别将它们配制成溶液,再进行焰色反应,观察火焰颜色 | |
| C. | 分别将它们配制成溶液,再加入BaCl2溶液,观察是否有沉淀产生 | |
| D. | 分别加热,再用澄清石灰水检验是否有气体产生 |
2.下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题.
(1)S原子结构示意图为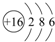 ;其最外层共有6种不同运动状态的电子;
;其最外层共有6种不同运动状态的电子;
(2)Na和Mg金属性较强的元素是Na(填元素符号),写出能证明这一结论的一个实验事实Na与水反应剧烈,Mg与水反应现象不明显;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填化学式),气态氢化物最稳定的是HCl(填化学式);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)Si是带来人类文明的重要元素之一,其氧化物是共价(填“离子”“共价”)化合物,常用于制造光导纤维(填一种高性能的现代通讯材料的名称).
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
 ;其最外层共有6种不同运动状态的电子;
;其最外层共有6种不同运动状态的电子;(2)Na和Mg金属性较强的元素是Na(填元素符号),写出能证明这一结论的一个实验事实Na与水反应剧烈,Mg与水反应现象不明显;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填化学式),气态氢化物最稳定的是HCl(填化学式);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)Si是带来人类文明的重要元素之一,其氧化物是共价(填“离子”“共价”)化合物,常用于制造光导纤维(填一种高性能的现代通讯材料的名称).
19.某主族元素R的最高正化合价与负化合价代数和为6,下列叙述正确的是( )
| A. | R一定是第VIIA族元素 | B. | R的最高价氧化物为RO3 | ||
| C. | R可能是第二周期元素 | D. | R的气态氢化物易溶于水显碱性 |
16.固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,同温下测得容器内压强不变,且反应后气体C的密度是原容器中气体密度的4倍.则下列判断正确的是( )
| A. | 生成的气体C为单质,且B和C的摩尔质量比为1:4 | |
| B. | 生成物C中A的质量分数为75% | |
| C. | 生成物C中A、B的原子个数比为3:1 | |
| D. | 反应前后气体分子数比为1:4 |
17.松花蛋于明朝初年问世.其腌制配方有多种,但主要配料为生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl).将一定比例的配料用水和粘土调 制成糊状,敷于蛋上,密封保存,数日后即可食用.
(1)松花蛋外的糊状物经水溶解、过滤,滤液中肯定大量含有的溶质它们是NaCl、NaOH,可能含有的物质为Ca(OH)2或Na2CO3.
(2)某同学设计如下表所示的实验方案,探究(1)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案.
(3)写出上表中可能发生反应的离子方程式:
①Ca2++CO32-=CaCO3↓
②CO32-+2H+=H2O+CO2↑.
(1)松花蛋外的糊状物经水溶解、过滤,滤液中肯定大量含有的溶质它们是NaCl、NaOH,可能含有的物质为Ca(OH)2或Na2CO3.
(2)某同学设计如下表所示的实验方案,探究(1)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案.
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| ①取少量滤液,滴加适量K2CO3溶液 | 有白色沉淀生成 | 滤液中含Ca(OH)2 |
| 无白色沉淀生成 | 滤液中无Ca(OH)2 | |
| ②另取少量滤液,加适量的稀盐酸 | 有无色气体逸出 | 滤液中含Na2CO3 |
| 无无色气体逸出 | 滤液中无Na2CO3 |
①Ca2++CO32-=CaCO3↓
②CO32-+2H+=H2O+CO2↑.