题目内容
17.关于氧化还原反应,下列说法正确的是( )①氧化剂发生氧化反应
②氧化剂具有氧化性
③某元素在反应中由化合物转化为单质,该元素一定被氧化
④物质所含元素化合价变化是判断氧化还原反应的依据
⑤失电子越多的还原剂,其还原性越强.
| A. | ②④ | B. | ②③④ | C. | ①②④ | D. | ②④⑤ |
分析 ①氧化剂化合价降低得电子;
②氧化剂得电子具有氧化性;
③某元素在反应中由化合物转化为单质,该元素的化合价可能升高,也可能降低;
④存在元素化合价变化的反应是氧化还原反应;
⑤还原性与失电子能力有关.
解答 解:①氧化还原反应中所含有元素化合价降低的物质为氧化剂,氧化剂化合价降低得电子,发生还原反应,故错误;
②氧化剂在反应中元素的化合价降低,得电子,具有氧化性,故正确;
③某元素在反应中由化合物转化为单质,该元素的化合价可能升高,也可能降低,元素可能被氧化,如Cl-→Cl2,也可能被还原,如Cu2+→Cu,故错误;
④存在元素化合价变化的反应是氧化还原反应,所以物质所含元素化合价变化是判断氧化还原反应的依据,故正确;
⑤还原性与失电子能力有关,与失电子数多少无关,越易失电子,还原性越强,故错误.
故选A.
点评 本题考查氧化还原反应,题目难度不大,本题注意从化合价的角度分析氧化还原反应,注意常见物质的性质,侧重氧化还原反应基本概念的考查.

练习册系列答案
相关题目
8.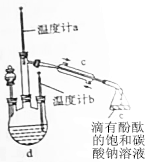 乙酸丁酯沸点、溶解性如下表.
乙酸丁酯沸点、溶解性如下表.
某研究行学习小组设计实验制取乙酸丁酯的方案,其主要步骤如下:
①在三颈瓶中d中加入按体积比1:4:4的比例配制浓硫酸、1-丁醇和乙酸的混合溶液.
②控制115-125℃均匀加热装有混合液的三颈瓶5-10min.
③待锥形瓶e收集到一定量的产物后停止加热,撤去锥形瓶e并用力振荡,然后静置待分层.
④分离出乙酸丁酯层,洗涤,干燥.
根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为:先加入丁醇,然后边摇动试管边慢慢加入浓硫酸,再加乙酸;写出制取乙酸丁酯的化学方程式:CH3COOH+CH3CH2OH $→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(2)上述实验中饱和碳酸钠溶液的作用是BC(填序号);
A.中和乙酸和1-丁醇
B.中和乙酸并吸收部分1-丁醇
C.乙酸丁酯在饱和碳酸钠溶液中的溶解度比在水中更小
D.加速酯的生成,提高其产率
(3)当温度计a(填写“a”或“b”)的温度读数达到126.3℃时,开始收集产品乙酸丁酯.
(4)指出步骤③所观察到的现象:在浅红色碳酸钠溶液层上方有无色液体出现,闻到香味,振荡后碳酸钠溶液层红色变浅;分离处乙酸丁酯后,一般用饱和食盐水和饱和氯化钙溶液洗涤,可通过洗涤除去(填名称)碳酸钠、乙醇杂质;为了干燥乙酸丁酯可选用的干燥剂为(填序号)B.
A.五氧化二磷 B.无水硫酸钠
C.碱石灰 D.氢氧化钠固体.
 乙酸丁酯沸点、溶解性如下表.
乙酸丁酯沸点、溶解性如下表.| 物质 | 乙酸 | 1-丁醇 | 乙酸丁酯 | 90%浓硫酸 |
| 沸点 | 117.9℃ | 117.2℃ | 126.3℃ | 338.0℃ |
| 溶解性 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 微溶于水,溶于有机溶剂 | 与水混溶 |
①在三颈瓶中d中加入按体积比1:4:4的比例配制浓硫酸、1-丁醇和乙酸的混合溶液.
②控制115-125℃均匀加热装有混合液的三颈瓶5-10min.
③待锥形瓶e收集到一定量的产物后停止加热,撤去锥形瓶e并用力振荡,然后静置待分层.
④分离出乙酸丁酯层,洗涤,干燥.
根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为:先加入丁醇,然后边摇动试管边慢慢加入浓硫酸,再加乙酸;写出制取乙酸丁酯的化学方程式:CH3COOH+CH3CH2OH $→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(2)上述实验中饱和碳酸钠溶液的作用是BC(填序号);
A.中和乙酸和1-丁醇
B.中和乙酸并吸收部分1-丁醇
C.乙酸丁酯在饱和碳酸钠溶液中的溶解度比在水中更小
D.加速酯的生成,提高其产率
(3)当温度计a(填写“a”或“b”)的温度读数达到126.3℃时,开始收集产品乙酸丁酯.
(4)指出步骤③所观察到的现象:在浅红色碳酸钠溶液层上方有无色液体出现,闻到香味,振荡后碳酸钠溶液层红色变浅;分离处乙酸丁酯后,一般用饱和食盐水和饱和氯化钙溶液洗涤,可通过洗涤除去(填名称)碳酸钠、乙醇杂质;为了干燥乙酸丁酯可选用的干燥剂为(填序号)B.
A.五氧化二磷 B.无水硫酸钠
C.碱石灰 D.氢氧化钠固体.
5.下列说法中正确的是( )
| A. | 氯化钠水溶液在电流的作用下电离出Na+和Cl- | |
| B. | 硫酸钡难溶于水,但硫酸钡属于强电解质 | |
| C. | 二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质 | |
| D. | 硫酸氢钠在水中的电离方程式可表示为NaHSO4═Na++HSO4- |
12.在汽车排气管加装催化装置,可有效减少CO和NOx的排放,催化装置内发生反应为:NOx+CO$\stackrel{催化剂}{→}$N2+CO2下列关于此反应的说法中错误的是( )
| A. | 等物质的量N2和CO2中,共用电子对的个数比为3:4 | |
| B. | 该反应中化合价变化的有N和C元素 | |
| C. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 | |
| D. | 当x=2时,每生成1mol N2,转移电子数为4mol |
2.NA代表阿伏伽德罗常数,下列说法正确的是( )
| A. | 1molNaCl固体溶于1L水所得溶液中NaCl的物质的量浓度为1mol•L-1 | |
| B. | 2.3g钠转化为钠离子时得到的电子数目为0.1NA | |
| C. | 常温常压下,11.2L 甲烷中所含的氢原子数为2NA | |
| D. | 32g O2和O3混合气体所含的原子数目为2NA |
9.实验室制取少量N2的反应是NaNO2+NH4Cl$\stackrel{△}{→}$NaCl+N2↑↑+2H2O,下列说法正确的是( )
| A. | NaNO2发生的是氧化反应 | B. | 生成1molN2时转移的电子数为3mol | ||
| C. | NH4Cl中的N元素被还原 | D. | N2既是氧化剂有事还原剂 |
7.下列各组说法一定正确的是( )
| A. | 强电解质:盐酸、氢氧化钡、明矾 | |
| B. | 纯净物:冰水混合物;含氧40%的氧化镁 | |
| C. | 有单质参加和单质生成的化学反应一定是氧化还原反应 | |
| D. | 同位素:H2、D2、T2 |