��Ŀ����
��14g���ۼ���500mL Fe2��SO4��3��CuSO4�Ļ����Һ�У���ַ�Ӧ�õ�ij��Һ��һ�������Ĺ��������
��1���ù����������һ������ ���ѧʽ��
��2����Ӧ����Һ��һ�������ڵ��� ��
A.2��ͭ����B.2��������C.3��������D�����������
��3������Ӧ��õ�500ml1mol/L��FeSO4��Һ��6g����������ԭ�����Һ��Fe2��SO4��3�����ʵ���Ũ��Ϊ ���������������Ϊ ��
��1���ù����������һ������
��2����Ӧ����Һ��һ�������ڵ���
A.2��ͭ����B.2��������C.3��������D�����������
��3������Ӧ��õ�500ml1mol/L��FeSO4��Һ��6g����������ԭ�����Һ��Fe2��SO4��3�����ʵ���Ũ��Ϊ
���㣺��ѧ����ʽ���йؼ���
ר�⣺������
��������1����2����������Fe3+��Cu2+����������ۣ��ȷ�����Ӧ��Fe+Fe2��SO4��3=3FeSO4���������Ӧ��Fe+CuSO4=FeSO4+Cu�����������һ����ͭ�����ܺ���Fe��Ҳ����û��Fe����Ӧ����Һ��һ��û��Fe3+��һ������Fe2+�����ܺ���Cu2+��
��3������FeSO4��Һ����Fe2��SO4��3��CuSO4����ȫ��Ӧ����ԭ��Һ��Fe2��SO4��3��CuSO4�����ʵ����ֱ�Ϊxmol��ymol�����ݷ���ʽ��ʾ�����ĵ�Fe�����ɵ�Cu��FeSO4�����ʵ���������FeSO4���ʵ����������������з��̼��㣬�ٸ���c=
����ԭ�����Һ��Fe2��SO4��3�����ʵ�����Ũ�ȣ�����ȷ��������ɣ�
��3������FeSO4��Һ����Fe2��SO4��3��CuSO4����ȫ��Ӧ����ԭ��Һ��Fe2��SO4��3��CuSO4�����ʵ����ֱ�Ϊxmol��ymol�����ݷ���ʽ��ʾ�����ĵ�Fe�����ɵ�Cu��FeSO4�����ʵ���������FeSO4���ʵ����������������з��̼��㣬�ٸ���c=
| n |
| V |
���
�⣺��1����������Fe3+��Cu2+����������ۣ��ȷ�����Ӧ��Fe+Fe2��SO4��3=3FeSO4���������Ӧ��Fe+CuSO4=FeSO4+Cu�������й����������������һ����ͭ�������������ܺ���Fe��Ҳ����û��Fe���ʴ�Ϊ��Cu��
��2����Ӧ������Һ��һ������FeSO4��û��Fe2��SO4��3������ȷ���Ƿ���CuSO4����Ӧ����Һ��һ��û��Fe3+��һ������Fe2+��SO42-�����ܺ���Cu2+����ѡ��C��
��3����ԭ��Һ��Fe2��SO4��3��CuSO4�����ʵ����ֱ�Ϊxmol��ymol����
Fe+Fe2��SO4��3=3FeSO4
xmol xmol 3xmol
Fe+CuSO4=FeSO4+Cu��
ymol ymol ymol ymol
������Һ��FeSO4���ʵ���Ϊ1mol/��0.5L=0.5mol����3x+y=0.5
����������Ϊ6g����14-56��x+y��+64y=6��
�������̣���ã�x=0.15��y=0.05��
��ԭ�����ҺFe2��SO4��3�����ʵ���Ũ��Ϊ��c[F2��SO4��3]=
=0.3mol/L��
����������Cu������Ϊ0.05mol��64g/mol=3.2g��ʣ��Fe������Ϊ6g-3.2g=2.8g����6g�������Ϊ3.2gCu��2.8gFe��
�ʴ�Ϊ��0.3mol/L��3.2gCu��2.8gFe��
��2����Ӧ������Һ��һ������FeSO4��û��Fe2��SO4��3������ȷ���Ƿ���CuSO4����Ӧ����Һ��һ��û��Fe3+��һ������Fe2+��SO42-�����ܺ���Cu2+����ѡ��C��
��3����ԭ��Һ��Fe2��SO4��3��CuSO4�����ʵ����ֱ�Ϊxmol��ymol����
Fe+Fe2��SO4��3=3FeSO4
xmol xmol 3xmol
Fe+CuSO4=FeSO4+Cu��
ymol ymol ymol ymol
������Һ��FeSO4���ʵ���Ϊ1mol/��0.5L=0.5mol����3x+y=0.5
����������Ϊ6g����14-56��x+y��+64y=6��
�������̣���ã�x=0.15��y=0.05��
��ԭ�����ҺFe2��SO4��3�����ʵ���Ũ��Ϊ��c[F2��SO4��3]=
| 0.15mol |
| 0.5L |
����������Cu������Ϊ0.05mol��64g/mol=3.2g��ʣ��Fe������Ϊ6g-3.2g=2.8g����6g�������Ϊ3.2gCu��2.8gFe��
�ʴ�Ϊ��0.3mol/L��3.2gCu��2.8gFe��
���������⿼��Ԫ�ػ��������ʼ����ƶϡ��������㣬�ؼ�����ȷ�����Ե�ǿ������Ӧ���Ⱥ�˳��3����ע��Fe2��SO4��3��CuSO4��ȫ��Ӧ���Ѷ��еȣ�

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ
���й���һ���ͷų��������ǣ�������
| A���û���Ӧ |
| B���ֽⷴӦ |
| C�����Ӳ��ԭ�� |
| D��ԭ����ɷ��� |


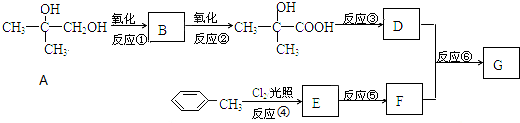


 ��·��������ʾ���밴Ҫ������
��·��������ʾ���밴Ҫ������