题目内容
下列有关结构和性质的说法中不正确的是( )
| A、元素周期表中从ⅢB族到ⅡB族十个纵行的元素都是金属元素 |
| B、碱性:NaOH>NH3?H2O,所以元素的金属性:Na>N |
| C、同周期第ⅡA族与第ⅢA族的元素原子序数之差不一定为1 |
| D、第ⅦA族元素从上到下,其氢化物的稳定性逐渐减弱 |
考点:同一主族内元素性质递变规律与原子结构的关系,元素周期律的作用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.元素周期表中从ⅢB族到ⅡB族十个纵行的元素为过渡金属元素;
B.比较金属性,应根据最高价氧化物对应的水化物的碱性;
C.第四周期相差11,第六周期相差25;
D.同主族元素从上到下元素的非金属性逐渐减弱.
B.比较金属性,应根据最高价氧化物对应的水化物的碱性;
C.第四周期相差11,第六周期相差25;
D.同主族元素从上到下元素的非金属性逐渐减弱.
解答:
解:A.元素周期表中从ⅢB族到ⅡB族十个纵行的元素为过渡金属元素,都为金属,故A正确;
B.比较金属性,应根据最高价氧化物对应的水化物的碱性,比较角度错误,故B错误;
C.第四周期相差11,第六周期相差25,故C正确;
D.同主族元素从上到下元素的非金属性逐渐减弱,非金属性越强,对应的氢化物越稳定,故D正确.
故选B.
B.比较金属性,应根据最高价氧化物对应的水化物的碱性,比较角度错误,故B错误;
C.第四周期相差11,第六周期相差25,故C正确;
D.同主族元素从上到下元素的非金属性逐渐减弱,非金属性越强,对应的氢化物越稳定,故D正确.
故选B.
点评:本题考查元素性质的递变规律,题目难度不大,本题注意把握元素周期律的递变规律,注意元素的性质与元素对应单质、化合物的性质的关系,把握比较物质性质的方法.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
在标准状况下,将V L A气体(摩尔质量M g/mol)溶于100ml水中(A与水不反应),所得A的水溶液密度为ρ g/cm3,则此溶液的物质的量浓度(mol/L)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
化学中常用图象直观地描述化学反应的进程或结果.下列对图象的叙述正确的是( )
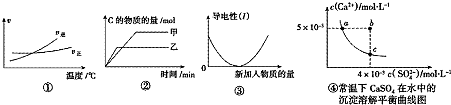

| A、根据图①可判断可逆反应A2(g)+3B2(g)?2AB2(g),正反应是吸热反应 |
| B、图②可表示压强对反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
| C、图③可表示乙酸溶液中通人氨气至过量的过程中溶液导电性的变化 |
| D、根据图④可知,a点对应的KSP等于c点对应的KSP |
下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 干冰 |
| B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
| C | 胆矾 | 盐酸 | 铁 | 碳酸钙 |
| D | 胆矾 | 水煤气 | 氯化铜 | 碳酸钠 |
| A、A | B、B | C、C | D、D |
某物质的结构简式为  ,其命名正确的是( )
,其命名正确的是( )
 ,其命名正确的是( )
,其命名正确的是( )| A、3-甲基-4-乙基-2-戊醇 |
| B、3,4-二甲基-5-己醇 |
| C、3,4-二甲基-2-己醇 |
| D、3-甲基-2-乙基-4-戊醇 |
某温度时,在体积为1L的密闭容器中,A、B、C三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,B的体积百分含量与时间关系如图Ⅱ所示.则下列结论正确的是( )
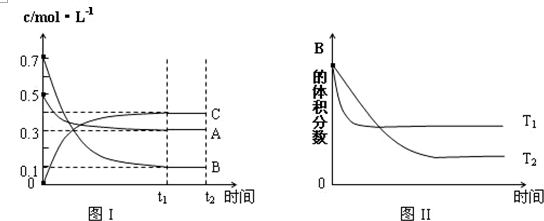

| A、该反应的热化学方程式为:A(g )+3B(g)?2C(g);△H>0 |
| B、达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
| C、达到平衡后,若其他条件不变,减小体积,平衡向逆反应方向移动 |
| D、若其它条件不变,升高温度,正、逆反应速率均增大,A的转化率减小 |
用铂丝蘸取氯化钠溶液在酒精灯上灼烧,火焰呈现黄色,显色原因是( )
| A、氯化钠受热挥发 |
| B、氯化钠受热分解 |
| C、钠离子中电子跃迁 |
| D、氯离子中电子跃迁 |
下列有机物命名正确的是( )
A、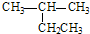 2-乙基丙烷 2-乙基丙烷 |
| B、CH3CH2CH2CH2OH 1-丁醇 |
C、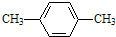 间二甲苯 间二甲苯 |
D、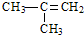 2-甲基-2-丙烯 2-甲基-2-丙烯 |
将14g铜银合金跟足量的某浓度HNO3反应,将放出的气体与1.12LO2(标准状况)混合,通入水中,恰好全部吸收,则合金中银的质量是( )
| A、3.2g | B、10.8g |
| C、21.6g | D、5.4g |