题目内容
下列各组中两种物质在溶液中的反应,能用同一离子方程式表示的是( )
| A、铁和稀盐酸、铁和稀醋酸 |
| B、FeCl3和NaOH、FeCl3和NH3?H2O |
| C、BaCl2+H2SO4; Ba(OH)2+Na2SO4 |
| D、NaHCO3+NaOH; NaHSO4+NaOH |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氯化氢为强电解质,拆成离子形式;醋酸为弱电解质,保留化学式;
B.氢氧化钠为强电解质,拆成离子形式;一水合氨为弱电解质,保留化学式;
C.反应的实质都是钡离子与硫酸根离子反应生成硫酸钡沉淀;
D.碳酸氢根离子为多元弱酸酸式根离子,不能拆;硫酸氢根离子为强酸酸式根离子,拆成氢离子和硫酸根离子.
B.氢氧化钠为强电解质,拆成离子形式;一水合氨为弱电解质,保留化学式;
C.反应的实质都是钡离子与硫酸根离子反应生成硫酸钡沉淀;
D.碳酸氢根离子为多元弱酸酸式根离子,不能拆;硫酸氢根离子为强酸酸式根离子,拆成氢离子和硫酸根离子.
解答:
解:A.铁和稀盐酸离子方程式为:Fe+2H+═Fe2++H2↑,铁和稀醋酸离子方程式为:Fe+2CH3COOH═Fe2++H2↑+2CH3COO-,故A错误;
B.FeCl3和NaOH反应的离子方程式为;Fe3++3OH-=Fe(OH)3↓;FeCl3和NH3?H2O离子方程式为:Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,故B错误;
C.BaCl2+H2SO4; Ba(OH)2+Na2SO4反应的实质都是钡离子与硫酸根离子反应生成硫酸钡沉淀,离子方程式都是:Ba2++SO42-=BaSO4↓,故C正确;
D.NaHCO3+NaOH,反应的离子方程式为:HCO3-+OH-=H2O+CO32-; NaHSO4+NaOH反应的离子方程式为:H++OH-=H2O,故D错误;
故选:C.
B.FeCl3和NaOH反应的离子方程式为;Fe3++3OH-=Fe(OH)3↓;FeCl3和NH3?H2O离子方程式为:Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,故B错误;
C.BaCl2+H2SO4; Ba(OH)2+Na2SO4反应的实质都是钡离子与硫酸根离子反应生成硫酸钡沉淀,离子方程式都是:Ba2++SO42-=BaSO4↓,故C正确;
D.NaHCO3+NaOH,反应的离子方程式为:HCO3-+OH-=H2O+CO32-; NaHSO4+NaOH反应的离子方程式为:H++OH-=H2O,故D错误;
故选:C.
点评:本题考查离子反应方程式书写的正误判断,明确反应的实质及书写离子方程式时需保留化学式的物质是解答本题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在反应 KClO3+6HCl=KCl+3Cl2↑+3H2O中,当生成1molCl2时转移电子的物质的量( )
| A、5mol |
| B、3 mol |
| C、5/3 mol |
| D、1 mol |
某溶液既能溶解Al(OH)3,又能溶解BaCO3且均形成溶液,在该溶液中可以大量共存的离子组是( )
| A、Fe3+、Mg2+、SO42-、NO3- |
| B、Ag+、Al3+、NO3-、OH- |
| C、Na+、Ba2+,Cl-、ClO- |
| D、K+、Na+、CO32-、NO3- |
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与盐酸的反应 2OH-+2H+=2H2O |
| B、澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O |
| C、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag |
| D、碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
下列说法正确的是( )
| A、强电解质一定是离子化合物,弱电解质一定是共价化合物 |
| B、强电解质一定是易溶于水的化合物,弱电解质一定是难溶于水的化合物 |
| C、CO2的水溶液导电能力很弱,所以CO2是弱电解质 |
| D、属于共价化合物的电解质在熔化状态下一般不导电 |

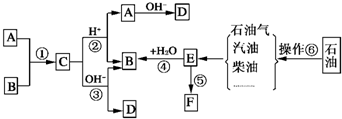 已知:A、B、F是家庭中常见的有机物,F常用于食品包装,E是石油化工发展水平的标志.根据下面转化关系回答问题.
已知:A、B、F是家庭中常见的有机物,F常用于食品包装,E是石油化工发展水平的标志.根据下面转化关系回答问题.