题目内容
14.0.5mol CO2的质量为22克,约含有9.03×1023个原子,11摩尔质子.分析 把0.5mol带入n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算CO2的质量和分子式,原子数为分子数的3倍,一个CO2含有的质子数为6+8×2=22.
解答 解:0.5mol CO2的质量m=0.5mol×44g/mol=22g,含有的分子数N=0.5mol×6.02×1023mol-1=3.01×1023,原子数为3×3.01×1023=9.03×1023,一个CO2含有的质子数为6+8×2=22,因此0.5mol CO2含有22×0.5mol=11mol质子,
故答案为:22;9.03×1023;11.
点评 本题考查了物质的量的相关计算,难度不大,带入计算时注意微粒的一致性.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
4.下列离子方程式书写正确的是( )
| A. | 铁粉加入稀盐酸中:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 铜片插入硝酸银溶液中:Cu+Ag+=Ag+Cu2+ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| D. | 氢氧化铝与稀硫酸反应:OHˉ+H+=H2O |
2.水处理包括水的净化、杀菌消毒、蒸馏等.其中常见的杀菌消毒剂包括氯气、臭氧、漂白粉、活性炭等.游泳场馆往往用臭氧、活性炭对游泳池进行消毒和净化.下列说法中正确的是( )
| A. | 臭氧、活性炭处理水的原理相同 | |
| B. | 氯气是一种常用的消毒剂,用氯气消毒的水也可以用于配制各种化学试剂 | |
| C. | 氯气和二氧化硫都具有漂白性,等体积的两者混合会提高漂白的效率 | |
| D. | 漂白粉长期露置在空气中会失效 |
9.生活处处有化学,下列说法正确的是( )
| A. | 石油主要是各种烷烃、环烷烃、烯烃组成的混合物 | |
| B. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| C. | 煎炸食物的花生油和牛油都是可皂化的酯类 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
6.下列各种物质中所含化学键种类最多的物质是( )
| A. | NaCl | B. | CaCl2 | C. | Br2 | D. | NH4Cl |
3.下列关于硫酸性质的描述中,正确的是( )
| A. | 浓H2SO4有强氧化性,稀H2SO4完全没有氧化性 | |
| B. | 由于浓H2SO4具有脱水性,所以可用做干燥剂 | |
| C. | 稀硫酸不与铜反应,但把Cu片放在浓H2SO4中立即发生激烈反应 | |
| D. | 在受热的情况下浓硫酸也能与铁、铝发生反应 |
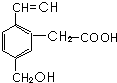 某有机物的结构为图所示,这种有机物不可能具有的性质是( )
某有机物的结构为图所示,这种有机物不可能具有的性质是( )