题目内容
粉末试样X是由Fe和Fe2O3组成的混合物.现进行如图1实验
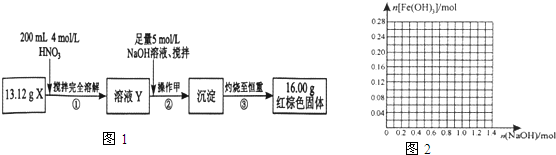
(1)操作甲的名称是
(2)X中Fe和Fe2O3物质的量之比为 .
(3)200mL溶液Y中存在多种阳离子,且在滴加NaOH溶液的过程中有刺激性气味的气体产生.已知在步骤①中,只收集到标准状况下896mL NO气体.请将溶液Y中存在的阳离子符号及其浓度填入下表.
(4)步骤①中发生的化学变化有多个,请写出其中任意一个反应的化学方程式: .
(5)请在图2中画出在200mL溶液Y中,加人NaOH物质的量与生成的Fe(OH)3物质的量的关系曲线.

(1)操作甲的名称是
(2)X中Fe和Fe2O3物质的量之比为
(3)200mL溶液Y中存在多种阳离子,且在滴加NaOH溶液的过程中有刺激性气味的气体产生.已知在步骤①中,只收集到标准状况下896mL NO气体.请将溶液Y中存在的阳离子符号及其浓度填入下表.
| 阳离子 | 阳离子浓度(mol/L) |
| H+ | 0.5 |
(5)请在图2中画出在200mL溶液Y中,加人NaOH物质的量与生成的Fe(OH)3物质的量的关系曲线.
分析:(1)流程分析②的操作甲是得到沉淀,操作为过滤;
(2)流程分析判断,最后得到的红褐色固体为Fe2O3,物质的量=
=0.1mol,依据铁元素守恒结合样品质量列式计算得到;
(3)200mL溶液Y中存在多种阳离子,且在滴加NaOH溶液的过程中有刺激性气味的气体产生,判断Y溶液中含有铵根离子,已知在步骤①中,只收集到标准状况下896mL NO气体,说明做氧化剂的硝酸物质的量=n(NO)=
=0.04mol,表格中氢离子物质的量=0.2L×0.5mol/L=0.1mol,说明剩余硝酸物质的量为0.1mol,依据得到的红褐色固体为氧化铁,计算得到铁元素物质的量为0.2mol,所以含有铁离子的浓度为1mol/L,结合溶液中电荷守恒计算铵根离子浓度;
(4)步骤1中可能是铁和吸收反应书写硝酸铁,一氧化氮和水,或铁和硝酸反应生成硝酸铁、硝酸铵和水,氧化铁和硝酸反应生成硝酸铁和水等反应;
(5)上述计算可知Fe3+物质的量,随加入氢氧化钠量的增多,氢氧化铁沉淀量增大,达到最大后不再变化,据此画出变化图象.
(2)流程分析判断,最后得到的红褐色固体为Fe2O3,物质的量=
| 16g |
| 160g/mol |
(3)200mL溶液Y中存在多种阳离子,且在滴加NaOH溶液的过程中有刺激性气味的气体产生,判断Y溶液中含有铵根离子,已知在步骤①中,只收集到标准状况下896mL NO气体,说明做氧化剂的硝酸物质的量=n(NO)=
| 0.896L |
| 22.4L/mol |
(4)步骤1中可能是铁和吸收反应书写硝酸铁,一氧化氮和水,或铁和硝酸反应生成硝酸铁、硝酸铵和水,氧化铁和硝酸反应生成硝酸铁和水等反应;
(5)上述计算可知Fe3+物质的量,随加入氢氧化钠量的增多,氢氧化铁沉淀量增大,达到最大后不再变化,据此画出变化图象.
解答:解:(1)依据流程分析②的操作甲是得到沉淀,实验操作为过滤操作,故答案为:过滤;
(2)最后得到的红褐色固体为Fe2O3,物质的量=
=0.1mol,铁元素物质的量为0.2mol,设样品中Fe物质的量为x,Fe2O3物质的量为y,得到:
x+2y=0.2
56x+160y=13.12
x=0.12mol
y=0.04mol
X中Fe和Fe2O3物质的量之比=0.12:0.04=3:1,
故答案为:3:1;
(3)200mL溶液Y中存在多种阳离子,且在滴加NaOH溶液的过程中有刺激性气味的气体产生,判断Y溶液中含有铵根离子,已知在步骤①中,只收集到标准状况下896mL NO气体,说明做氧化剂的硝酸物质的量=n(NO)=
=0.04mol,做氧化剂的硝酸为水层一氧化氮和铵根离子的硝酸,表格中氢离子物质的量=0.2L×0.5mol/L=0.1mol,说明剩余硝酸物质的量为0.1mol,依据得到的红褐色固体为氧化铁,计算得到铁元素物质的量为0.2mol,所以含有铁离子的浓度为1mol/L,结合溶液中电荷守恒计算铵根离子浓度,溶液中硝酸根离子物质的量=0.2×4-0.04-c(NH4+)×0.2,c(HNO3)=1×4-0.2-(NH4+)×1,
c(H+)+c(NH4+)+3c(Fe3+)=c(NO3-),0.5+c(NH4+)+1×3=1×4-0.2-c(NH4+)×1,c(NH4+)=0.15mol/L,
故答案为:Fe3+;1;NH4+;0.15mol;
(4)计算得到铁元素物质的量为0.2mol,生成最大量氢氧化铁沉淀为0.2mol,随加入氢氧化钠溶液增多达到最大量沉淀后,沉淀质量不再变化,据此画出好图象为: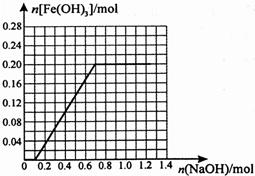 ,
,
故答案为: .
.
(2)最后得到的红褐色固体为Fe2O3,物质的量=
| 16g |
| 160g/mol |
x+2y=0.2
56x+160y=13.12
x=0.12mol
y=0.04mol
X中Fe和Fe2O3物质的量之比=0.12:0.04=3:1,
故答案为:3:1;
(3)200mL溶液Y中存在多种阳离子,且在滴加NaOH溶液的过程中有刺激性气味的气体产生,判断Y溶液中含有铵根离子,已知在步骤①中,只收集到标准状况下896mL NO气体,说明做氧化剂的硝酸物质的量=n(NO)=
| 0.896L |
| 22.4L/mol |
c(H+)+c(NH4+)+3c(Fe3+)=c(NO3-),0.5+c(NH4+)+1×3=1×4-0.2-c(NH4+)×1,c(NH4+)=0.15mol/L,
故答案为:Fe3+;1;NH4+;0.15mol;
(4)计算得到铁元素物质的量为0.2mol,生成最大量氢氧化铁沉淀为0.2mol,随加入氢氧化钠溶液增多达到最大量沉淀后,沉淀质量不再变化,据此画出好图象为:
 ,
,故答案为:
 .
.点评:本题考查了实验探究物质性质和产物组成的分析判断,元素守恒的计算应用,氧化还原反应电子守恒的计算分析,溶液中离子种类判断,电荷守恒的计算,题目难度较大.

练习册系列答案
相关题目
