题目内容
17.利用某含铬废液[含较低浓度的Na2Cr2O7、Fe2(SO4)3]制备K2Cr2O7.流程如下:
Ⅰ.用NaOH溶液调pH至3.6,产生红褐色沉淀,过滤;
Ⅱ.向滤液中加入Na2SO3,一定操作后分离出Na2SO4;
Ⅲ.将分离出Na2SO4后得到的溶液调pH约为5,得到Cr(OH)3沉淀;
Ⅳ.在KOH存在条件下,向Cr(OH)3中加入足量H2O2溶液,得到黄色溶液;
Ⅴ.向黄色溶液中加入物质A后,溶液变为橙红色,一定操作后得到K2Cr2O7固体;
Ⅵ.测定K2Cr2O7固体的纯度.
已知:Cr2O72-(橙红色)+H2O2CrO42-(黄色)+2H+
(1)步骤Ⅰ中红褐色沉淀的化学式是Fe(OH)3.
(2)步骤Ⅱ中加入Na2SO3的目的是将Cr2O72-还原为Cr3+.
(3)步骤Ⅳ中反应的离子方程式是2Cr(OH)3+3H2O2+4OH-=2CrO42-+8H2O.
(4)步骤Ⅴ中加入的物质A可以是c.(填序号)
a.KOH b.K2CO3 c.H2SO4 d.SO2
(5)步骤Ⅵ的操作是:取0.45g K2Cr2O7产品配成溶液,酸化后滴入18.00mL 0.50mol/L
的FeSO4溶液,恰好使Cr2O72-完全转化为Cr3+.产品中K2Cr2O7的质量分数是98%.(注:K2Cr2O7的摩尔质量为294g/mol)
分析 因废液中含有Fe3+,滴加NaOH调节溶液pH时会生成Fe(OH)3红褐色沉淀,达到除去溶液里Fe3+的目的,然后加入亚硫酸钠溶液将溶液里的将+6价的Cr还原为+3价,然后将Cr3+转化为Cr(OH)3沉淀,再通过氧化和酸化两个过程即得到目标产物,最后利用滴定法测定产品的纯度,
(1)根据沉淀的颜色判断;
(2)Na2SO3具有还原性,具有氧化性Na2Cr2O7;
(3)Cr(OH)3与H2O2反应生成生成CrO42-;
(4)酸性条件下CrO42-转化为Cr2O72-;
(5)Fe2+使Cr2O72-完全转化为Cr3+,反应为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,根据方程式计算出的K2Cr2O7物质的量和质量,再求出纯度.
解答 解:(1)用NaOH溶液调pH至3.6,产生红褐色沉淀,则该沉淀为Fe(OH)3,故答案为:Fe(OH)3;
(2)Na2SO3具有还原性,具有氧化性Na2Cr2O7,向滤液中加入Na2SO3,发生氧化还原反应,将+6价的Cr还原为+3价,
故答案为:将Cr2O72-还原为Cr3+;
(3)在KOH存在条件下,向Cr(OH)3中加入足量H2O2溶液,Cr(OH)3与H2O2反应生成生成CrO42-,反应的离子方程式为:2Cr(OH)3+3H2O2+4OH-=2CrO42-+8H2O;
故答案为:2Cr(OH)3+3H2O2+4OH-=2CrO42-+8H2O;
(4)向黄色溶液中加入物质A后,溶液变为橙红色,一定操作后得到K2Cr2O7固体,在酸性条件下CrO42-转化为Cr2O72-,说明A为酸,则A可以是硫酸,故选c;
故答案为:c;
(5)Fe2+使Cr2O72-完全转化为Cr3+,反应为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,已知18.00mL 0.50mol/L的FeSO4溶液,
则K2Cr2O7物质的量为:$\frac{1}{6}$×0.018L×0.50mol/L=0.0015mol,其质量为0.0015mol×294g/mol=0.441g,
其纯度为$\frac{0.441g}{0.45g}$×100%=98%;
故答案为:98%.
点评 本题综合考查物质的制备,为高频考点和常见题型,题目涉及氧化还原反应、离子方程式的书写、根据方程式的计算、化学平衡移动等问题,题目难度中等,本题注意从质量守恒的角度利用关系式法计算,难度中等.

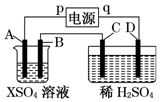 如图所示,p、q为直流电源的两极,A由金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D上产生气泡,试回答:
如图所示,p、q为直流电源的两极,A由金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D上产生气泡,试回答:(1)p为正极,A极发生了氧化反应.
(2)C为阳极,可收集到氧气;D为阴极,可收集到氢气.
(3)C极的电极反应式为4OH--4e-=O2↑+2H2O.
(4)在电解过程中,测C、D两极上产生气体的体积,实验数据如表:
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极产生气体的体积(cm3) | 6 | 12 | 20 | 29 | 39] | 49 | 59 | 69 | 79 | 89 |
| 阳极产生气体的体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
(5)当反应进行一段时间后,A、B电极附近溶液的pH不变(填“增大”“减小”或“不变”).
(6)当电路中通过0.004mol电子时,B极上沉积的金属X为0.128g,则此金属的摩尔质量为64g/mol.
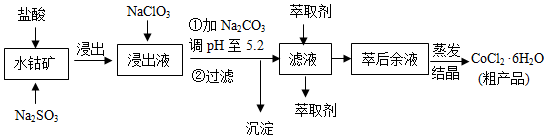
已知:
①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加Na2CO3调pH至5.2”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3,加入萃取剂的目的是除去溶液中的Mn2+.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
| A. | m+n<p | B. | 平衡向逆反应方向移动 | ||
| C. | A的转化率降低 | D. | C的体积分数增加 |
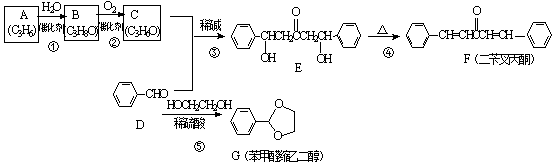
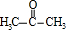 ;A加聚产物的结构简式是
;A加聚产物的结构简式是 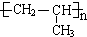 .
.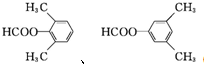 .
.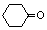 (环已酮)合成
(环已酮)合成 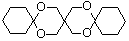 [已知HCHO是所有醛中还原性最强的(常用Ca(OH)2催化剂)]
[已知HCHO是所有醛中还原性最强的(常用Ca(OH)2催化剂)]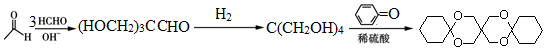 .
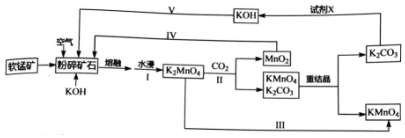
.
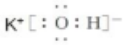 .
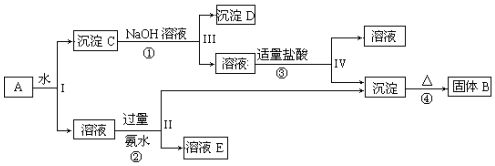
.
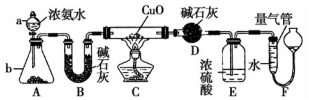 某课外活动小组欲利用CuO与NH4反应,研究NH3的某种性质并测定其组成,设计了如图实验装置(夹持装置未画出)进行实验.请回答下列问题:
某课外活动小组欲利用CuO与NH4反应,研究NH3的某种性质并测定其组成,设计了如图实验装置(夹持装置未画出)进行实验.请回答下列问题: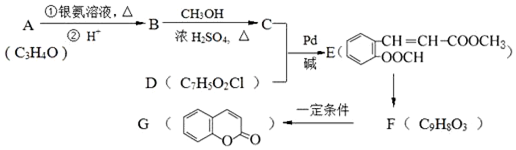

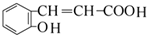 .
.
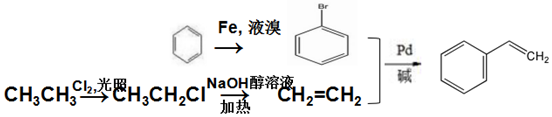 .
.