题目内容
20.在元素周期表短周期元素中,X元素与Y、Z、W三元素相邻.X、Y的原子序数之和等于Z的原子序数,这四种元素原子的最外层电子数之和为20.下列判断一定正确的是( )| A. | 单质熔点:Z>W | B. | 离子半径:X<Y | ||
| C. | X和Z可存在于同一离子化合物中 | D. | 氧化物对应水化物的酸性X>Z |
分析 在周期表中X与Y、Z、W紧密相邻,X、Y的原子序数之和等于Z的原子序数,所以X和Z属于同一主族且Z在X的下一周期,原子序数不大于18,设X的原子序数是a,则a+a+1=a+8,得a=7,或a-1+a=a+8,得a=9.若a=7,则X是N,Y是O,Z是P,又X、Y、Z、W四种短周期元素原子的最外层电子数之和为20,所以W是C,符合题意;若a=9,则X是F,Y是O,Z是Cl,三种元素原子的最外层电子数之和为20,不合题意,以此解答该题.
解答 解:在周期表中X与Y、Z、W紧密相邻,X、Y的原子序数之和等于Z的原子序数,所以X和Z属于同一主族且Z在X的下一周期,原子序数不大于18,设X的原子序数是a,则a+a+1=a+8,得a=7,或a-1+a=a+8,得a=9.若a=7,则X是N,Y是O,Z是P,又X、Y、Z、W四种短周期元素原子的最外层电子数之和为20,所以W是C,符合题意.若a=9,则X是F,Y是O,Z是Cl,三种元素原子的最外层电子数之和为20,不合题意;
所以X、Y、Z、W分别是N、O、P、C元素,
A.W如为金刚石,则熔点较高,故A错误;
B.X、Y对应的离子具有相同的核外电子排布,核电荷数越大离子半径越小,核电荷数X<Y,则离子半径:X>Y,故B错误;
C.X和Z可存在于磷酸铵中,故C正确;
D.非金属性N>P,元素的非进行性越强,对应的最高价氧化物的酸性越强,没有指出最高价,则酸性强弱不一定,故D错误;
故选C.
点评 本题考查原子结构和元素周期律关系,侧重考查分析、推断能力,涉及物质结构、基本概念、元素周期律,正确推断元素是解本题关键,题目难度中等.

练习册系列答案
相关题目
8.NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 标况下,22.4LSO3含有σ键数目为3NA | |
| B. | 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,则某容器内加入0.5 NA个N2(g)与足量的H2(g),充分反应后放出的热量为46 kJ | |
| C. | 标准状况下,22.4L氦气含有的原子数为2NA | |
| D. | 0.1mol HCN分子中含有的π键数目为0.2NA |
15.如表是元素周期表一部分,列出了十种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是Ca(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),呈两性的氢氧化物是Al(OH)3(填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键、共价键;
(4)用电子式表示元素③与⑧形成化合物的过程 .
.
(5)写出⑤与NaOH反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(6)写出工业冶炼⑤的化学方程式:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2第二步:Br2+SO2+2H2O=4H++SO42-+2Br-; 第三步Cl2+2Br-=2Cl-+Br2.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)在③~⑦元素中,原子半径最大的是Ca(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),呈两性的氢氧化物是Al(OH)3(填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键、共价键;
(4)用电子式表示元素③与⑧形成化合物的过程
 .
.(5)写出⑤与NaOH反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(6)写出工业冶炼⑤的化学方程式:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2第二步:Br2+SO2+2H2O=4H++SO42-+2Br-; 第三步Cl2+2Br-=2Cl-+Br2.
5.丁苯橡胶的结构简式如下: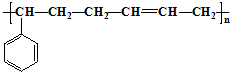 合成这种橡胶的单体应是( )
合成这种橡胶的单体应是( )
①苯乙烯 ②苯丙烯 ③2-丁烯 ④丙炔 ⑤1,3-丁二烯.
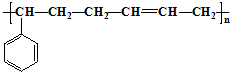 合成这种橡胶的单体应是( )
合成这种橡胶的单体应是( )①苯乙烯 ②苯丙烯 ③2-丁烯 ④丙炔 ⑤1,3-丁二烯.
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | ①⑤ |
12.生活中常见的聚酯纤维(的确良)的结构简式如图所示: .它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )
.它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )
 .它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )
.它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 3:1 |
9.为了除去酸性氯化铝溶液中的Cu2+,下列实验步骤顺序和所用试剂都正确的是( )
①通过量CO2;②加盐酸;③加过量NaOH溶液;④加AlCl3; ⑤过滤.
①通过量CO2;②加盐酸;③加过量NaOH溶液;④加AlCl3; ⑤过滤.
| A. | ③⑤④⑤② | B. | ③⑤② | C. | ③⑤①② | D. | ③⑤①⑤② |
10.下列说法不正确的是( )
| A. | 在氢原子的电子云图中,每个小黑点代表一个电子 | |
| B. | 某基态原子3d能级中电子排布的情况可能为 | |
| C. | 电子构型为[Ar]3d104s2的元素是过渡金属元素 | |
| D. | 当碳原子的核外电子排布由1s22s22p2转变为1s22s12p3时,碳原子由基态变为激发态 |