题目内容
W、X,Y,Z均为短周期元素,X,Y处于同一周期,X,Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构.下列说法正确的是( )
| A、原子最外层电子数:X>Y>Z |
| B、单质沸点:X>Y>Z |
| C、离子半径:X2->Y+>Z- |
| D、原子序数:X>Y>Z |
考点:原子结构与元素周期律的关系,真题集萃
专题:元素周期律与元素周期表专题
分析:X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,X、Y同周期,则X为S元素,结合元素在周期表中的位置以及元素周期律知识解答该题.
解答:
解:X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,X、Y同周期,则X为S元素,
A.X、Y、Z分别为S、Na、F,原子最外层电子数分别为6、1、7,故A错误;
B.常温下Na、S为固体,F2为气体,Na的熔点较低,但钠的沸点高于硫,顺序应为Na>S>F2,故B错误;
C.Na+、F-具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为F->Na+,故C错误;
D.X、Y、Z原子序数分别为16、11、9,原子序数:X>Y>Z,故D正确.
故选D.
A.X、Y、Z分别为S、Na、F,原子最外层电子数分别为6、1、7,故A错误;
B.常温下Na、S为固体,F2为气体,Na的熔点较低,但钠的沸点高于硫,顺序应为Na>S>F2,故B错误;
C.Na+、F-具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为F->Na+,故C错误;
D.X、Y、Z原子序数分别为16、11、9,原子序数:X>Y>Z,故D正确.
故选D.
点评:本题考查原子结构与元素周期律的关系,为高考常见题型,侧重于学生的分析能力的考查,题目难度不大,本题的关键是根据原子结构特点正确推断元素的种类.

练习册系列答案
相关题目
甲、乙两烧杯中各盛有200mL的相同浓度的盐酸和氢氧化钠溶液,向两烧杯中分别各加入5.4g的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则盐酸的物质的量浓度为( )
| A、1mol/L |
| B、1.5mol/L |
| C、2mol/L |
| D、2.5mol/L |
如图装置或操作能达到相应实验目的是( )
| A | B | C | D |
 | 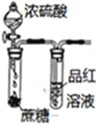 | 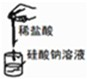 | 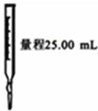 |
| 实验室利用氯化铵制取并收集NH3 | 说明浓H2SO4有脱水性、酸性、氧化性,SO2有漂白性 | 验证非金属性Cl>C>Si | 量取0.1mol?L-1KOH溶液20.00mL |
| A、A | B、B | C、C | D、D |
下列化合物中同分异构体数目最少的是( )
| A、戊烷 | B、戊醇 |
| C、戊烯 | D、乙酸乙酯 |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C2H4 CH4 |
| C、C60 C2H4 |
| D、NH3 HCl |
下列试剂中,标签上应标注 和
和 的是( )
的是( )
 和
和 的是( )
的是( )| A、C2H5OH |
| B、HNO3 |
| C、NaOH |
| D、HCl |
M3+有2个电子层,则M在元素周期表中的位置是( )
| A、第2周期0族 |
| B、第2周期Ⅷ族 |
| C、第3周期ⅢA族 |
| D、第3周期ⅡA族 |
下列叙述不正确的是( )
| A、Na、Mg、Al最外层电子数依次增多,其单核离子的氧化性依次增强 |
| B、N、O、F最高正价依次升高,对应的气态氢化物的稳定性依次增强 |
| C、第三周期元素的原子半径中,位于ⅦA族元素的最小 |
| D、Na、Mg、Al三种元素对应的氢氧化物的碱性依次减弱 |
下列各物质n(n≥3、自然数)相同时,其同类物质的同分异构体最多的是( )
| A、CnH2n+2O 醇 |
| B、CnH2nO 醛 |
| C、CnH2nO2 酸 |
| D、CnH2n+2 烃 |