题目内容
 过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:
过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:(1)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体转化为二氧化碳和水,达到无害化.有关甲醛、苯、二氧化碳及水说法正确的是
①苯与B3N3H6的总电子数相等;
②甲醛、苯分子中碳原子均采用sp3杂化;
③苯、二氧化碳、水和甲醛都是非极性分子;
④水的沸点比甲醛高得多,是因为水分子间能存在氢键,甲醛分子间不存在氢键.
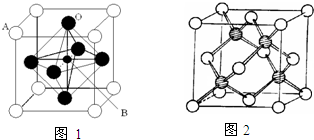
(2)2007年诺贝尔物理学奖为法国科学家阿尔贝?费尔和德国科学家彼得?格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就.某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应.
①用A、B、O表示这类特殊晶体的化学式:
②Cr、Mn的核外特征电子排布式分别为:Cr:[Kr]3d54s1、Mn:[Kr]3d54s2,则它们第一电离能由小到大的排列顺序是:
(3)CO2的空间构型为
(4)冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图2)类似,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有
考点:晶胞的计算,判断简单分子或离子的构型,晶体的类型与物质熔点、硬度、导电性等的关系,极性分子和非极性分子,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)①.苯中电子总数为6×6+6=42,B3N3H6电子总数为3×5+3×7+6=42,所以苯与B3N3H6电子总数相等;
②.甲醛、苯分子中碳原子均含有3个δ键,没有孤对电子,采用sp2杂化;
③.甲醛分子的空间结构不对称属于极性分子,水分子中氧原子有孤对电子,也是极性分子;
④.水的沸点比甲醛高得多,是因为水分子间能形成氢键;
(2)①利用均摊法计算晶体的化学式;
②因为Cr的电子排布式为:[Kr]3d54s1,Mn的电子排布式为:[Kr]3d54s2,锰与铬在同一周期且锰的原子序数大于铬,根据元素周期律可知,第一电离能由小到大的排列顺序是Cr<Mn;
(3)根据价层电子对互斥理论确定其空间构型,根据不同类型晶体的性质差异进行比较熔沸点;
(4)利用均摊法确定每个冰晶胞含有的水分子个数,根据氧原子和碳原子的杂化方式分析.
②.甲醛、苯分子中碳原子均含有3个δ键,没有孤对电子,采用sp2杂化;
③.甲醛分子的空间结构不对称属于极性分子,水分子中氧原子有孤对电子,也是极性分子;
④.水的沸点比甲醛高得多,是因为水分子间能形成氢键;
(2)①利用均摊法计算晶体的化学式;
②因为Cr的电子排布式为:[Kr]3d54s1,Mn的电子排布式为:[Kr]3d54s2,锰与铬在同一周期且锰的原子序数大于铬,根据元素周期律可知,第一电离能由小到大的排列顺序是Cr<Mn;
(3)根据价层电子对互斥理论确定其空间构型,根据不同类型晶体的性质差异进行比较熔沸点;
(4)利用均摊法确定每个冰晶胞含有的水分子个数,根据氧原子和碳原子的杂化方式分析.
解答:
解:(1))①.苯中电子总数为6×6+6=42,B3N3H6电子总数为3×5+3×7+6=42,所以苯与B3N3H6电子总数相等,故①正确;
②.甲醛、苯分子中碳原子均含有3个δ键,没有孤对电子,采用sp2杂化,故②错误;
③.甲醛分子的空间结构不对称属于极性分子,水分子中氧原子有孤对电子,也是极性分子,故③错误;
④.水的沸点比甲醛高得多,是因为水分子间能形成氢键,故④正确;
故答案为:①④;
(2)①由图1可知,晶胞中A位于顶点,晶胞中含有A为8×
=1个,B位于晶胞的体心,含有1个,O位于面心,晶胞中含有O的个数为6×
=3,则化学式为ABO3,
故答案为:ABO3;
②因为Cr的电子排布式为:[Kr]3d54s1,Mn的电子排布式为:[Kr]3d54s2,锰与铬在同一周期且锰的原子序数大于铬,根据元素周期律可知,第一电离能由小到大的排列顺序是Cr<Mn,故答案为:Cr<Mn;
(3)二氧化碳分子中碳原子价层电子对个数是2,且不含孤电子对,所以其空间构型是直线形,CO2是分子晶体,分子间是范德华力,SiO2是空间网状的原子晶体,原子之间是共价键,作用力远大于范德华力,所以固体CO2的熔沸点比SiO2熔沸点要小得多,
故答案为:直线型分子;CO2是分子间作用力形成的分子晶体,SiO2是共价键形成的空间网状原子晶体;
(4)每个冰晶胞平均占有分子个数=4+
×8+6×
=8,H2O的氧原子中含有2个σ键和2个孤电子对,金刚石中每个碳原子含有4个σ键且没有孤电子对,所以水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子中一个氧原子可以和另外2个水分子形成2个原子,2个氢原子可以和另外2个水分子形成氢键,所以每个水分子可与相邻的4个水分子形成氢键,导致冰晶胞与金刚石晶胞微粒排列方式相似,
故答案为:8;水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子可与相邻的4个水分子形成氢键,且为正四面体结构.
②.甲醛、苯分子中碳原子均含有3个δ键,没有孤对电子,采用sp2杂化,故②错误;
③.甲醛分子的空间结构不对称属于极性分子,水分子中氧原子有孤对电子,也是极性分子,故③错误;
④.水的沸点比甲醛高得多,是因为水分子间能形成氢键,故④正确;
故答案为:①④;
(2)①由图1可知,晶胞中A位于顶点,晶胞中含有A为8×
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:ABO3;
②因为Cr的电子排布式为:[Kr]3d54s1,Mn的电子排布式为:[Kr]3d54s2,锰与铬在同一周期且锰的原子序数大于铬,根据元素周期律可知,第一电离能由小到大的排列顺序是Cr<Mn,故答案为:Cr<Mn;
(3)二氧化碳分子中碳原子价层电子对个数是2,且不含孤电子对,所以其空间构型是直线形,CO2是分子晶体,分子间是范德华力,SiO2是空间网状的原子晶体,原子之间是共价键,作用力远大于范德华力,所以固体CO2的熔沸点比SiO2熔沸点要小得多,
故答案为:直线型分子;CO2是分子间作用力形成的分子晶体,SiO2是共价键形成的空间网状原子晶体;
(4)每个冰晶胞平均占有分子个数=4+
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:8;水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子可与相邻的4个水分子形成氢键,且为正四面体结构.
点评:本题主要考查了原子的杂化方式、分子的空间构型、不同类型晶体的性质、晶胞的计算等知识,有一定的综合性,中等难度.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关说法中正确的是( )
| A、乙烯使溴水、酸性高锰酸钾溶液褪色的原理相同 |
| B、乙醇可被直接氧化生成乙酸且乙醇与都能与单质钠反应 |
| C、淀粉、蔗糖、葡萄糖、蛋白质在稀硫酸中均能发生水解反应 |
| D、淀粉和聚乙烯都是天然的高分子化合物 |
下列分子或离子中键角由大到小排列顺序是( )
①BF3 ②NH3 ③H2O ④NH4+ ⑤BeCl2.
①BF3 ②NH3 ③H2O ④NH4+ ⑤BeCl2.
| A、⑤④①②③ |
| B、⑤①④②③ |
| C、④①②⑤③ |
| D、③②④①⑤ |

 如图是某中学实验室的一瓶硫酸试剂标签上的部分内容.
如图是某中学实验室的一瓶硫酸试剂标签上的部分内容.


