题目内容
(12分)用中和滴定法测定某烧碱样品的纯度。有以下步骤:
(1)配制待测液:用5.00 g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000 mL溶液。除烧杯、胶头滴管、玻璃棒外,还需要的玻璃仪器有__ _。
(2)滴定:
①盛装0.1000 mol·L-1盐酸标准液应该使用_________式滴定管。
②滴定时眼睛应 。
③有关数据记录如下:
(3)计算:烧碱样品的纯度是_________________。
(4)误差分析(选填“偏高”“偏低”或“无影响”):
①用蒸馏水冲洗锥形瓶,则会使测定结果___________;
②读数时,滴定前仰视,滴定后俯视,则会使测定结果___________。
(1)配制待测液:用5.00 g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000 mL溶液。除烧杯、胶头滴管、玻璃棒外,还需要的玻璃仪器有__ _。
(2)滴定:
①盛装0.1000 mol·L-1盐酸标准液应该使用_________式滴定管。
②滴定时眼睛应 。
③有关数据记录如下:
| 测定序号 | 待测溶液的体积/mL | 所耗盐酸标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
(4)误差分析(选填“偏高”“偏低”或“无影响”):
①用蒸馏水冲洗锥形瓶,则会使测定结果___________;
②读数时,滴定前仰视,滴定后俯视,则会使测定结果___________。
(1)1 000 mL容量瓶
(2)①酸 ②注视锥形瓶中溶液颜色的变化
(3)80.8%
(4)①无影响 ②偏低
(2)①酸 ②注视锥形瓶中溶液颜色的变化
(3)80.8%
(4)①无影响 ②偏低
考查中和滴定实验操作
(1)配制溶液最主要的仪器是特定规格的容量瓶
(2)盐酸应用酸式滴定管来盛装;滴定时眼睛注视锥形瓶中溶液颜色的变化;
(3)采用多次测定求平均值的方法,标准液的体积分别为:,20.28ml、20.12ml,平均为20.20ml;则待测液中NaOH的物质的量为: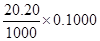 mol,烧碱样品中NaOH的物质的量为:
mol,烧碱样品中NaOH的物质的量为: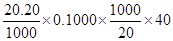 =4.04g,样品纯度为:
=4.04g,样品纯度为: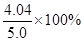 =80.8%。
=80.8%。
(4)锥形瓶只需要用蒸馏水洗涤干净即可,对测定结果无影响
②滴定前仰视,滴定后俯视均使标准液体积偏小,则会使测定结果偏低。
(1)配制溶液最主要的仪器是特定规格的容量瓶
(2)盐酸应用酸式滴定管来盛装;滴定时眼睛注视锥形瓶中溶液颜色的变化;
(3)采用多次测定求平均值的方法,标准液的体积分别为:,20.28ml、20.12ml,平均为20.20ml;则待测液中NaOH的物质的量为:
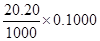 mol,烧碱样品中NaOH的物质的量为:
mol,烧碱样品中NaOH的物质的量为: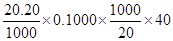 =4.04g,样品纯度为:
=4.04g,样品纯度为: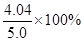 =80.8%。
=80.8%。(4)锥形瓶只需要用蒸馏水洗涤干净即可,对测定结果无影响
②滴定前仰视,滴定后俯视均使标准液体积偏小,则会使测定结果偏低。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
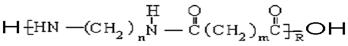 的单体为___________
的单体为___________ 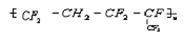 合成它的单体为________________________
合成它的单体为________________________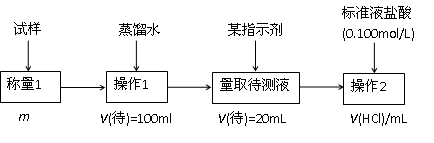

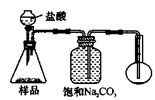
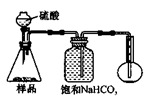


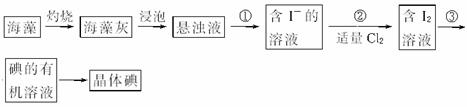
 适量___________ (填序号)溶液,反应的离子方程式为______________________。
适量___________ (填序号)溶液,反应的离子方程式为______________________。
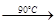 NH4ClO4(aq)+NaCl(aq)
NH4ClO4(aq)+NaCl(aq)