题目内容
13.汽车尾气(含CO、SO2和NO等)是城市空气污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转化器”,它能使一氧化碳跟一氧化氮反应生成可参与大气生态循环的无毒气体,并促进二氧化硫的转化.(1)汽车尾气中导致酸雨形成的主要物质是SO2、NO.
(2)写出在催化剂的作用下CO跟NO反应的化学方程式:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
(3)使用“催化转化器”的缺点是在一定程度上提高了排放废气的酸度,有可能促进了酸雨的形成,其原因是由于促进了SO2的转化,生成的SO3增多,SO3+H2O═H2SO4提高了空气酸度.
(4)下列各项措施中,有利于缓解城市空气污染的有ABC(填序号).
A.充分利用太阳能,减少能源消耗
B.使用电动车辆,减少汽油消耗
C.植树种草,绿化环境.
分析 (1)导致酸雨的气体有二氧化硫和氮的氧化物;
(2)CO与NO反应,生成可参与大气生态环境循环的无毒气体,并在催化剂作用下促使SO2的转化,可知CO与NO反应生成的是N2和CO2,由此即可写出有关化学方程式.
(3)由SO2可催化氧化为SO3,SO3在空气中能形成H2SO4,这也就是“催化转化器”的缺点.
(4)植树造林没有缓解城市空气污染,应该是使用清洁能源和不使用产生污染的能源才行.
解答 解:(1)因导致酸雨的气体有二氧化硫和氮的氧化物,汽车尾气中含CO、SO2和NO等,所以导致酸雨形成的主要物质是SO2和NO,故答案为:SO2、NO;
(2)根据题给信息:CO与NO反应,生成可参与大气生态环境循环的无毒气体.这气体是CO2和N2,所以反应的方程式为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2,
故答案为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2;
(3)由于“催化转化器”促进了SO2的转化,生成的SO3增多,SO3+H2O=H2SO4,提高了空气的酸度.
故答案为:由于促进了SO2的转化,生成的SO3增多,SO3+H2O═H2SO4提高了空气酸度;
(4)缓解城市空气污染,植树造林能 控制CO2量的增加,而对消除汽车尾气中烃类,故答案为:ABC.
点评 本题以汽车尾气处理这一生活常识为背景材料编写的信息题,为高频考点,侧重于化学与生活的考查,注意用很简单的化学知识加以解释.因此,我们要多关心与化学知识相关系的生产、生活中的热点问题,做到学以致用,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
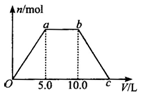 向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如图所示,试回答:
向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如图所示,试回答: