题目内容
1.下列实验中,所选装置合理的是( )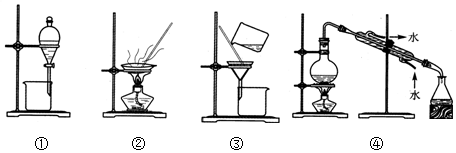
| A. | 装置①用于分离苯和水 | |
| B. | 装置②用于分离乙醇中的水 | |
| C. | 装置③用于分离FeCl3和Fe(SCN)3 | |
| D. | 装置④用于分离氯化钠和氯化铵固体 |
分析 A.苯不溶于水,溶液分层;
B.乙醇易挥发;
C.FeCl3和Fe(SCN)3都溶于水;
D.蒸馏用于分离沸点不同的液体混合物.
解答 解:A.苯不溶于水,溶液分层,可用分液的方法分离,故A正确;
B.乙醇与水的沸点不同,应用蒸馏的方法分离,如蒸发,乙醇易挥发,不能达到分离的目的,故B错误;
C.FeCl3和Fe(SCN)3都溶于水,不能用过滤的方法分离,故C错误;
D.蒸馏用于分离沸点不同的液体混合物,可用力氯化铵加热易分解,且氯化氢和氨气易生成氯化铵的性质分离,故D错误.
故选A.
点评 本题综合考查物质的分离、提纯,为高考常见题型,侧重考查学生的分析、实验能力,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
9.我国三峡工程所提供的清洁、廉价、强劲、可再生能源--水电,相当于每年燃烧3000万吨原煤的火力发电厂产生的电能,三峡工程有助于控制( )
①温室效应 ②形成酸雨 ③空气中的固体颗粒浓度 ④白色污染.
①温室效应 ②形成酸雨 ③空气中的固体颗粒浓度 ④白色污染.
| A. | 只有① | B. | 只有①② | C. | ②③④ | D. | ①②③ |
10.常温下,Ka(CH3COOH)=Kb(NH3•H2O)=1.75×10-5,下列说法正确的是( )
| A. | 用0.1mol•L-1的盐酸滴定0.1mol•L-1的氨水时,可用酚酞作指示剂 | |
| B. | 0.2 mol•L-1的醋酸与0.1 mol•L-1的氢氧化钠溶液等体积混合,所得溶液中:c(CH3COO-)+c(OH-)=C(CH3COOH)+C(H+) | |
| C. | pH=3的醋酸与pH=11的氨水等体积混合,所得溶液中有水电离出的C(H+)=1×10-7 mol•L-1 | |
| D. | pH=3的盐酸与pH=11的氨水等体积混合,所得溶液中C(NH3•H2O)>C(NH4+)>C(Cl-) |
9.已知还原性SO32->I-.某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等.向该无色溶液中滴加少量溴水,溶液仍呈无色.下列关于该溶液的判正确的是( )
| A. | 肯定不含I- | B. | 肯定含有Na+ | ||
| C. | 肯定不含SO42-肯定含有SO32- | D. | 不能肯定是否含有SO42 |
16.电解水时,为了增强水的导电性且电解过程中pH保持不变,应加入的物质是( )
| A. | H2SO4 | B. | NaOH | C. | Na2SO4 | D. | CuCl2 |
6. 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )| A. | a 电极发生反应:H2NCH2CH2NH2+16e-+4H2O═2CO2↑+N2↑+16H+ | |
| B. | 质子交换膜处H+由右向左移动 | |
| C. | 该电池在微生物作用下将化学能转化为电能 | |
| D. | 开始放电时b极附近pH不变 |
13.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 50mL18mol•L-1浓硫酸与足量铜供热,转移电子数为0.9NA | |
| C. | 0.1molCl2通入含0.1molFeBr2溶液中,被氧化的溴离子数为0.2NA | |
| D. | 标准状况下,2.24LNO和足量O2反应生成物中含有NO2分子数为0.1NA |
10.某柔性燃料电池(以甲醇为燃料,酸性介质)结构示意如图.下列有关说法正确的是( )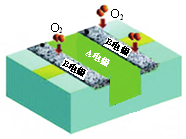

| A. | 电池工作时,电子由A电极经外电路流向B电极 | |
| B. | 电池工作时,减少的化学能完全转化为电能 | |
| C. | A电极发生的电极反应为:CH3OH-6e-+H2O═CO2+6H+ | |
| D. | B电极每消耗1 mol O2,电池中减少4 mol H+ |
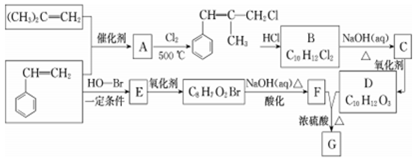
 .G的结构简式为
.G的结构简式为 .
.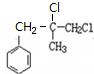 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$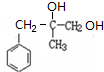 +2NaCl.
+2NaCl.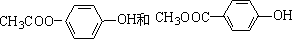 .
.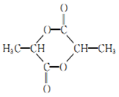 的合成路线:
的合成路线: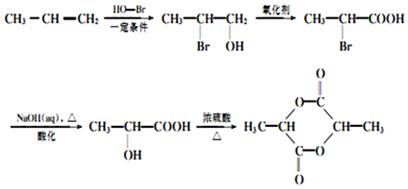 .
.