题目内容
H+浓度相同的两种一元酸HX和HY溶液,分别取100mL加入足量的镁粉,充分反应后,收集到H2的体积分别为V(HX)和V(HY),在相同条件下,V(HX)>V(HY),则下列说法正确的是( )
| A、HX可能是强酸 |
| B、HY一定是强酸 |
| C、HX的酸性强于HY的酸性 |
| D、反应开始时二者生成氢气的速率相同 |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:因开始的pH相同,镁足量,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,反应速率与氢离子浓度成正比,以此进行分析并解答.
解答:
解:A.pH=l的两种一元酸HX与HY溶液,分别与足量Mg反应,HX产生氢气多,则HX为弱酸,故A错误;
B.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,二者可能一种为强酸,另一种为弱酸,或者二者都是弱酸,其中HX较弱,故B错误;
C.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,故C错误;
D.反应开始时,两种溶液中氢离子浓度相等,所以反应速率相同,故D正确;
故选D.
B.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,二者可能一种为强酸,另一种为弱酸,或者二者都是弱酸,其中HX较弱,故B错误;
C.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,故C错误;
D.反应开始时,两种溶液中氢离子浓度相等,所以反应速率相同,故D正确;
故选D.
点评:本题考查弱电解质在溶液中的电离,题目难度不大,本题要注意两种酸的强弱比较的角度,不能确定是否一定是强酸.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
密闭容器中有如下反应:mA(g)+nB(g)?pC(g)达到平衡后,保持温度不变,将容器体积缩小到原来的
,当达到新平衡时,C的浓度为原来的1.8倍.下列说法中正确的是( )
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率降低 |
| C、平衡向正反应方向移动 |
| D、C的质量分数增加 |
Na2O和Na2O2的下列叙述中正确的是( )
| A、Na2O比Na2O2稳定 |
| B、均可与CO2、H2O反应产生氧气 |
| C、Na2O是淡黄色固体,而Na2O2是白色固体 |
| D、阴阳离子个数比均为1:2 |
下列说法中错误的是( )
| A、钠在空气中燃烧时,先熔化,再燃烧,产物为Na2O2 |
| B、镁在空气中形成一层致密的氧化膜,故镁不需要像钠那样的特殊保护 |
| C、铝制品在生活中非常普遍,是因为铝不活泼 |
| D、铁在潮湿的空气中生成的氧化物疏松多孔,不能保护内层金属,故铁制品往往需要涂保护层 |
温度为T时,向4.0L恒容密闭容器中充入2.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A、反应在前50 s的平均速率为v(PCl3)=0.0064 mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol?L-1,则反应的△H<0 |
| C、相同温度下,起始时向容器中充入4.0molPCl3、4.0molCl2,达到平衡时,PCl3的转化率等于80% |
| D、相同温度下,起始时向容器中充入2.0molPCl5、0.40molPCl3和0.40molCl2,达到平衡前v(正)<v(逆) |
NO2通过盛有水的洗气瓶,转移0.02mol电子时,参加反应的NO2气体在标准状况下的体积为( )
| A、224mL |
| B、336mL |
| C、448mL |
| D、672mL |
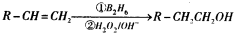
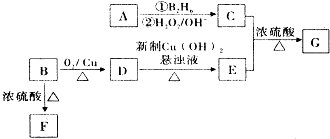
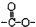 ”基团.
”基团.