题目内容
铜的摩尔质量为M g/mol,密度为d g/cm3,阿伏加德罗常数为NA,下列说法正确的是( )
| A、1kg铜所含原子的数目为dNA | ||
B、一个铜原子所占有的体积为(
| ||
C、一个铜原子的质量为
| ||
D、1dm3铜所含有的原子数为
|
考点:阿伏加德罗定律及推论
专题:
分析:A.根据n=
计算出铜的物质的量,再根据N=nNA计算出铜原子的数目;
B.1个铜原子的物质的量为:
mol,根据m=nM计算出1个铜原子的质量,再根据V=
计算出一个铜原子所占有的体积;
C.1个铜原子的物质的量为
mol,然后根据m=nM计算出1个铜原子的质量;
D.根据m=ρV计算出铜的质量,再根据n=
计算出铜的物质的量,最后根据N=nNA计算出铜原子的数目.
| m |
| M |
B.1个铜原子的物质的量为:
| 1 |
| NA |
| m |
| ρ |
C.1个铜原子的物质的量为
| 1 |
| NA |
D.根据m=ρV计算出铜的质量,再根据n=
| m |
| M |
解答:
解:A.1kg铜的物质的量为:
=
mol,所含铜原子数为:
NA,故A错误;
B.1个铜原子的物质的量为:
mol,则1个铜原子的质量为:
mol×Mg/mol=
g,所以一个铜原子所占有的体积为:
=
cm3,故B错误;
C.1个铜原子的物质的量为:
mol,则1个铜原子的质量为:
mol×Mg/mol=
g,故C正确;
D.1dm3铜的质量是1000d g,铜的物质的量为:
mol,所以含原子数目为
NA,故D错误;
故选C.
| 1000g |
| Mg/mol |
| 1000 |
| M |
| 1000 |
| M |
B.1个铜原子的物质的量为:
| 1 |
| NA |
| 1 |
| NA |
| M |
| NA |
| ||
| dg?cm3 |
| M |
| dNA |
C.1个铜原子的物质的量为:
| 1 |
| NA |
| 1 |
| NA |
| M |
| NA |
D.1dm3铜的质量是1000d g,铜的物质的量为:
| 1000d |
| M |
| 1000d |
| M |
故选C.
点评:本题考查了阿伏伽德罗定律及推论的应用,题目难度中等,注意掌握阿伏伽德罗定律的内容,明确物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系,试题培养了学生的计算能力.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
浩瀚的海洋中蕴藏着丰富的资源,其中可以为人类利用的氯化物含量相当高.海水中含量最多的氯化物是( )
| A、NaCl |
| B、MgCl2 |
| C、KCl |
| D、CaCl2 |
下列各组物质的关系中,其中属于同分异构体的是( )
| A、O2 和O3 |
| B、16O 和18O |
| C、正丁烷和异丁烷 |
| D、甲烷和乙烷 |
将0.56g铁粉加入到25mL2mol?L-1的氯化铁溶液中,充分反应后,其结果是( )
| A、氧化产物与还原产物的物质的量之比为2:1 |
| B、铁粉剩余,溶液呈浅绿色,Cl-基本不变 |
| C、向溶液中滴入无色KSCN溶液,仍无色 |
| D、Fe2+和Fe3+物质的量之比为1:1 |
能区分胶体和溶液的实验方法是( )
| A、静置,有沉淀现象的是胶体 |
| B、有丁达尔现象的是胶体 |
| C、不能透过滤纸的是胶体 |
| D、用肉眼观察,均一、透明的是溶液 |
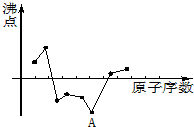
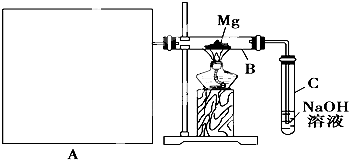 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.