题目内容
5.某有机化合物A的相对分子质量范围为100~130.经分析得知,其中碳和氢的质量分数之和为46.66%,其余为氧,则该化合物分子中最多含碳氧双键的个数为( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 根据含氧量和相对分子质量的范围,得出氧原子数,根据氧元素的质量分数进而求得有机化合物的相对分子质量,从而计算化学式.
解答 解:有机物中碳和氢的质量分数之和为46.66%,所以氧的质量分数为53.34%,由化合物A的相对分子质量大于100,小于130,
所以氧原子个数为大于$\frac{100×0.5334}{16}$=3.33,小于$\frac{130×0.5334}{16}$=4.33,所以氧原子为4个,
所以有机物分子质量=$\frac{4×16}{0.5334}$=120,
其中C、H的相对原子质量之和为120-16×4=56,除以12得到4余8,所以碳氢部分为C4H8,可确定分子式为C4H8O4,
C4H8O4与4个C原子的饱和衍生物(可表示为C4H10On)比较可知,有一个不饱和度,即分子中最多含有1个碳氧双键,
故选A.
点评 本题考查有机物分子式的确定,题目难度不大,注意计算氧原子数为解答该题的关键.

练习册系列答案
相关题目
16.下列物质属于由共价键形成的化合物的是( )
| A. | H2 | B. | CaCl2 | C. | C2H6 | D. | KF |
13.下列关于醇和酚的说法中,正确的是( )
| A. | 在水中乙醇和苯酚都不能电离 | |
| B. | 分子内有苯环和羟基的化合物一定是酚 | |
| C. | 苯甲醇与2-甲基苯酚互为同分异构体 | |
| D. | 酚和醇具有相同的官能团,因而具有相同的化学性质 |
20.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16mol CO2和3.6g H2O的混合气体.下列说法正确的是( )
| A. | 没有乙烷 | B. | 一定是甲烷和乙烯 | ||
| C. | 有甲烷 | D. | 有乙炔 |
10.在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K与温度t的关系如表:
(1)该反应的化学平衡常数表达式为K=$\frac{[CO]•[{H}_{2}O]}{[C{O}_{2}]•[{H}_{2}]}$.
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是ad.
a、混合气体中c(CO)不变 b、容器中压强不变
c、c(CO2)=c(CO) d、v正(H2)=v逆(H2O)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O)试判断此时的温度为950℃.
(5)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度c(CO2)为2mol•L-1,c(H2)为1.5mol•L-1,c(CO)为1mol•L-1,c(H2O)为3mol•L-1则下一时刻,反应将逆向(填“正向”或“逆向”)进行.
CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K与温度t的关系如表:
| t℃ | 700 | 800 | 950 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是ad.
a、混合气体中c(CO)不变 b、容器中压强不变
c、c(CO2)=c(CO) d、v正(H2)=v逆(H2O)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O)试判断此时的温度为950℃.
(5)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度c(CO2)为2mol•L-1,c(H2)为1.5mol•L-1,c(CO)为1mol•L-1,c(H2O)为3mol•L-1则下一时刻,反应将逆向(填“正向”或“逆向”)进行.
17.为纪念俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔.该元素最稳定的一定原子为${\;}_{101}^{258}$Md,该原子的中子数为( )
| A. | 101 | B. | 258 | C. | 157 | D. | 359 |
14.已知拆开1mol氢气中的化学键需要消耗436.4KJ能量,拆开1mol氧气中的化学键需要消耗498KJ能量,形成水分子中的1molH-O键能够释放462.8KJ能量,则反应2H2(g)+O2(g)=2H2O(g)的能量变化是( )
| A. | 吸收445.2KJ | B. | 吸收480.4KJ | C. | 放出445.2KJ | D. | 放出480.4KJ |
15.如图所示原电池装置中,电解质溶液为硫酸,下列有关叙述错误的是( )
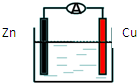

| A. | 锌做负极发生氧化反应 | |
| B. | 供电时的总反应为:Zn+2H+=Zn2++H2↑ | |
| C. | 该装置可实现化学能转化为电能 | |
| D. | 溶液中硫酸根离子向Cu极移动 |