题目内容
4.某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量.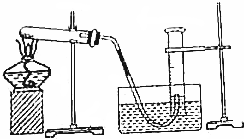
实验步骤如下:①组装好实验装置,检查装置的气密性;②把适量的氯酸钾粉末和少量的二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为a g;③加热,开始反应,直到产生一定量的气体;④停止加热(如图,导管出口高于液面),并测量收集到的气体的体积;⑤准确称量试管和残留物的质量为b g.回答下列问题:
(1)如何检查装置的气密性?将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后有少量水进入导管,表明不漏气
(2)以下是测量收集到的气体体积必须包括的几个步骤.
①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积.这三步操作的正确顺序是②①③(填步骤代号).
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同?慢慢将量筒下移
(4)如果实验中得到的氧气体积是cL(已折算为标准状况),水蒸气的影响忽略不计,氧气的摩尔质量为(可用含a、b、c的式子表示)$\frac{22.4(a-b)}{c}$g/mol.
分析 (1)通过气体发生器与液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;一般用到的方法有:空气热胀冷缩法、注水法等;据此解答;
(2)从气体的热胀冷缩和读量筒中气体体积的方法两方面进行分析;
(3)观察装置图可知,量筒内液面高于水槽液面,只要将量筒慢慢下移即可,从气体的热胀冷缩和读量筒中气体体积的方法两方面进行分析;
(4)依据标况下的氧气体积是cL,计算氧气的质量和物质的量,依据M=$\frac{m}{n}$计算.
解答 解:(1)装置气密性检查方法:将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后有少量水进入导管,表明不漏气;
故答案为:将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后有少量水进入导管,表明不漏气;
(2)要准确测量气体体积必须保持量筒内外气体的温度和压强相等,因此在读取量筒内气体的体积之前,应使试管和量筒内的气体都冷却至室温;再调节量筒内外液面高度使之相同,所以正确的顺序为:②①③;
故答案为:②①③;
(3)试管和量筒内的气体都冷却后,量筒内的液面一定高于量筒外的液面,慢慢将量筒下移,量筒上方气体体积减小,压强增大,当量筒内气体压强等于外界大气压时,量筒内液面和水槽内液面相平;
故答案为:慢慢将量筒下移;
(4)标况下,Vm=22.4L/mol,则氧气的物质的量n=$\frac{cL}{22.4L/mol}$,氧气的质量=(a-b)g;
依据M(O2)=$\frac{m}{n}$=$\frac{(a-b)g;}{\frac{cL}{22.4L/mol}}$=$\frac{22.4(a-b)}{c}$(g/mol);
故答案为:$\frac{22.4(a-b)}{c}$.
点评 本题为实验题,侧重考出制取气体装置气密性检验、气体体积测量方法,熟悉基本实验操作是解题关键,题目难度不大.

| A. | 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA | |
| B. | 常温常压下,1mol氦气含有的原子数为2NA | |
| C. | 1molAl3+含有核外电子数为10NA | |
| D. | 17gNH3含有的电子数为10NA |
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是K,非金属最强的元素是F;(填写元素符号)
(3)表中能形成两性氢氧化物的元素是Al,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O,Al(OH)3+KOH=KAlO2+2H2O;
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱(用化学方程式表达):Cl2+2NaBr=Br2+2NaCl.
| A. | 农村用酸汤点豆腐 | B. | 有雾的清晨树林里的阳光 | ||
| C. | 澄清石灰水在空气中放置后变浑浊 | D. | 铁盐用于净水 |
| A. | Fe2++Cl2→Fe3++2Cl- | |
| B. | 2Fe2++2Br-+2I-+3Cl2=2Fe3++I2+Br2+6Cl- | |
| C. | 2Fe2++4Br-+2I-+4Cl2→2Fe3++I2+2Br2+8Cl- | |
| D. | 4Fe2++2Br-+2I-+4Cl2=4Fe3++I2+Br2+8Cl- |
