题目内容
下列说法不正确的是( )
| A、燃煤中加入适量石灰石可以减少SO2的排放 |
| B、淀粉和纤维素互为同分异构体 |
| C、酚醛塑料具有热固性,可做烹饪器材的手柄 |
| D、橡胶硫化可以提高橡胶的强度和韧性 |
考点:二氧化硫的化学性质,同分异构现象和同分异构体,有机高分子化合物的结构和性质
专题:化学应用
分析:A.二氧化硫与石灰石分解生成的CaO反应生成亚硫酸钙;
B.淀粉和纤维素的分子式不同;
C.酚醛塑料为网状结构;
D.橡胶硫化中存在硫的交联结构.
B.淀粉和纤维素的分子式不同;
C.酚醛塑料为网状结构;
D.橡胶硫化中存在硫的交联结构.
解答:
解:A.二氧化硫与石灰石分解生成的CaO反应生成亚硫酸钙,从而减少SO2的排放,故A正确;
B.淀粉和纤维素均表示为(C6H10O5)n,n不同,则分子式不同,二者不是同分异构体,故B错误;
C.酚醛塑料为网状结构,具有热固性,可做烹饪器材的手柄,故C正确;
D.橡胶硫化中存在硫的交联结构,则提高橡胶的强度和韧性,故D正确;
故选B.
B.淀粉和纤维素均表示为(C6H10O5)n,n不同,则分子式不同,二者不是同分异构体,故B错误;
C.酚醛塑料为网状结构,具有热固性,可做烹饪器材的手柄,故C正确;
D.橡胶硫化中存在硫的交联结构,则提高橡胶的强度和韧性,故D正确;
故选B.
点评:本题考查物质的性质,为高频考点,综合性较强,把发生的反应及有机物的结构与性质、用途的关系等为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
短周期元素A、B、C、D的原子序数依次增大.A原子的最外层电子数是内层电子数的2倍,元素B在同周期的主族元素中原子半径最大,元素C的合金是日常生活中常用的金属材料,D位于第VIA族.下列说法正确的是( )
| A、原子半径:D>B>C>A |
| B、元素A、B的氧化物具有相同类型的化学键 |
| C、元素B和C的最高价氧化物对应水化物的碱性:B>C |
| D、B、C、D的最高价氧化物对应的水化物能相互反应 |
下列事实能用同一原理解释的是( )
| A、Na2O2和活性炭均能使品红溶液褪色 |
| B、对碘晶体和碳酸氢铵晶体加热,晶体均会逐渐消失 |
| C、SO2能使滴加酚酞的NaOH溶液和酸性KMnO4溶液的红色都褪去 |
| D、实验室配制FeC13溶液和SnC12溶液时,先将固体FeC13和SnCl2分别溶解在浓盐酸中,再加蒸馏水稀释 |
下列实验室制备气体的说法正确的是( )
| A、制备氯气,可以用MnO2与稀盐酸反应 |
| B、制备氨气,可以用浓硫酸干燥 |
| C、制备HI,可以用浓硫酸与NaI反应 |
| D、制备SO2,可以用NaOH溶液进行尾气吸收 |
NA代表阿伏加德罗常数的数值,下列叙述正确的是( )
| A、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,转移4NA个电子 |
| B、1.0L 1.0mol/L NaAlO2水溶液中含有的氧原子数为2NA |
| C、标准状况下分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶粒微粒数为NA |
下列四种工业生产,不需用石灰石作为一种原料的是( )
| A、用海水为原料制镁 |
| B、冶炼生铁 |
| C、制漂白粉 |
| D、铝土矿中提取铝 |
关于物质的用途说法错误的是( )
| A、甲烷是家用天然气的主要成分 |
| B、氯气可用于制取漂白粉 |
| C、晶体硅是制造光导纤维的主要原料 |
| D、碳酸氢钠可作发酵剂 |
T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的 浓度变化如图(Ⅰ)所示.保持其它条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示,下列结论正确的是( )
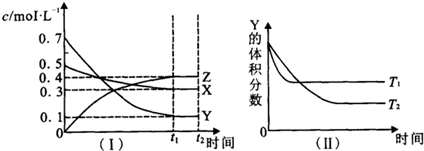

| A、图(Ⅱ)中T1>T2,则正反应是吸热反应 |
| B、t2 min时,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、其它条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大 |
| D、T℃时,若密闭容器中各物质起始浓度为:0.4mol?L-1 X、0.4mol?L-1 Y、0.2mol/L Z保持其他条件不变,达到平衡时z的浓度为0.4 mol?L-1 |