题目内容
11.在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反应mX(g)+nY(g)?pZ(g)△H=Q kJ/mol.反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如表所示.下列说法不正确的是( )| 容器体积/L c(Y)/(mol•L-1) 温度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
| A. | m+n>p | |
| B. | Q<0 | |
| C. | 体积不变,温度升高,平衡向逆反应方向移动 | |
| D. | 温度不变,压强增大,Y的质量分数增大 |
分析 根据题目信息可得,在温度相同的条件下,当体积扩大到原来的两倍时,Y的浓度降低的倍数小于2,所以可确定增大体积,平衡逆向移动,根据平衡移动原理,增大体积,平衡向体积增大的方向移动,当体积相同时,温度升高,Y的浓度增大,即平衡正向移动,所以此反应的正向为吸热反应,以此解答该题.
解答 解:A.在温度相同的条件下,当体积扩大到原来的两倍时,Y的浓度降低的倍数小于2,所以可确定增大体积,平衡逆向移动,则m+n<p,故A错误;
B.当体积相同时,温度升高,Y的浓度增大,即平衡正向移动,所以此反应的正向为吸热反应,则Q>0,故B错误;
C.反应的正向为吸热反应,体积不变,温度升高,平衡正向移动,故C错误;
D.温度不变,压强增大,平衡向逆反应方向移动,则Y的质量分数增大,故D正确.
故选D.
点评 本题考查化学平衡的影响,为高频考点,侧重考查学生的分析能力,题目主要通过控制变量讨论化学平衡移动问题,对于学生的基本功要求较高,题目难度中等.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
1.能证明氢氟酸是弱酸的实验事实是( )
| A. | HF溶液与Zn反应放出H2 | B. | 0.1mol/LNaF溶液的pH大于7 | ||
| C. | HF溶液与Na2CO3反应生成CO2 | D. | 0.1mol/LHF溶液可使紫色石蕊变红 |
2.依据如图判断,下列说法正确的是( )
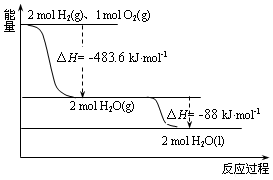

| A. | 氢气的燃烧热△H=-241.8 kJ•mol-1 | |
| B. | 2 mol H2(g)与1 mol O2(g)所具有的总能量比2 mol H2O(g) 所具有的总能量低 | |
| C. | 液态水分解的热化学方程式为:2H2O(l)=2H2(g)+O2(g)△H=+571.6 kJ•mol-1 | |
| D. | H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量 |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol丙烯酸中含有的双键数目为0.1 NA | |
| B. | 常温常压下,4.6 g NO2和N2O4的混合气体中分子总数为0.3 NA | |
| C. | 标准状况下,2.24 L Cl2与足量水反应转移的电子数目为0.1 NA | |
| D. | 7.8 g Na2O2固体中含有的离子总数为0.3 NA |
6.下列物质性质与应用对应关系正确的是( )
| A. | 氢氟酸显弱酸性,可用于雕刻玻璃 | |
| B. | NaClO溶液显碱性,可用于杀菌消毒 | |
| C. | NH4Cl分解时吸收大量的热,可用作阻燃剂 | |
| D. | CO2密度比空气大,可用作镁着火时的灭火剂 |
16.NA表示阿伏伽德罗常数的值,下列叙述不正确的是( )
| A. | 标准状况下22.4L水含有的分子数为NA | |
| B. | 0.5mol氢气中氢原子数为6NA | |
| C. | 常温下5.6g铁与足量盐酸反应失去的电子数为0.2NA | |
| D. | 标准状况下22.4LCO2与CO的混合气体含分子数为NA |
3.用NA表示阿伏伽德罗常数的数值,下列叙述正确的是( )
| A. | 标准状况下,22.4L由O2、和NO2组成的混合气体含有的原子数为2NA | |
| B. | 1mol羟基与1mol氢氧根离子含有的电子数均为9NA | |
| C. | 0.1molFe2+与足量H2O2溶液反应,转移的电子数为0.1NA | |
| D. | 1L1 mol•L-1NaF溶液中含有F-的数目为NA |
1.下列实验设计,不能达到实验目的是( )
| A. | 用CCl4将溴从溴水中提取出来 | |
| B. | 向某无色溶液中加入硝酸银产生白色沉淀,证明溶液中含有Cl- | |
| C. | 采用加热的方法除去氯化钠固体中混有的氯化铵固体 | |
| D. | 用丁达尔效应鉴别淀粉胶体和食盐溶液 |