题目内容
3.将20g A、20g B及20g C混合,完全反应后,得9g B,24.5g C,还有D.已知D的摩尔质量为106g•mol-1.现将44g A和44g B反应,生成D的物质的量为( )| A. | 0.5mol | B. | 0.55mol | C. | 1mol | D. | 2mol |
分析 将20g A、20g B及20g C混合,完全反应后,得9g B,24.5g C,则20gA完全反应,参加反应的B的质量为:20g-9g=11g,生成的C的质量为:24.5g-20g=4.5g,根据质量守恒定律计算生成的D的质量,根据质量守恒定律,判断44g A和44g B反应,哪种物质有剩余,根据不足量的物质利用质量定比关系计算生成D的质量,再根据n=$\frac{m}{M}$计算生成的D的物质的量.
解答 解:将20g A、20g B及20g C混合,完全反应后,得9g B,24.5g C,则20gA完全反应,参加反应的B的质量为:20g-9g=11g,生成的C的质量为:24.5g-20g=4.5g,
根据质量守恒定律可知,生成的D的质量为:60g-9g-24.5g=26.5g,
44gB完全反应需要A的质量为:20g×$\frac{44g}{11g}$=80g,大于44g,则44g A和44g B反应时,A不足会完全反应,反应生成D的质量为:26.5g×$\frac{44}{20}$=58.3g,
故生成D的物质的量为:$\frac{58.3g}{106g/mol}$=0.55mol,
故选B.
点评 本题考查化学方程式的计算,题目难度中等,明确发生反应实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题有利于提高学生的分析能力及化学计算能力.

练习册系列答案
相关题目
2. 通过化学加工使煤转化为气体、液体、固体燃料,工业上用CO和H2合成CH3OH,请回答下列问题.
通过化学加工使煤转化为气体、液体、固体燃料,工业上用CO和H2合成CH3OH,请回答下列问题.
(1)恒容密闭容器中,将水蒸气通过红热的炭,产生水煤气.反应为C(s)+H2O(g)?CO(g)+H2(g),除升高温度、使用催化剂外,能够使该反应速率增大的措施有增大H2O(g)的浓度.
(2)将不同量的CO(g)和H2O(g)分别通入到容积为2L的恒容密闭容器中,进行下列反应CO(g)+H2O(g)?CO2(g)+H2(g),得到数据如下:
①反应CO(g)+H2O?CO2(g)+H2(g)的△H<0(填“>”、“=”、“<”).
②实验2中,v(CO2)=0.125mol•L-1•min-1,n=3;
③实验2和实验3中CO的转化率关系为:前者等于后者(填“大于”、“等于”、“小于”).
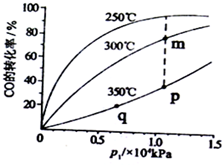
(3)工业上用CO(g)+2H2(g)?CH3OH(g)合成(CH3OH)具有重要意义.把一定物质的量的反应物投料于一恒容容器中,测得不同温度下CO转化率与温度和压强的关系,根据如图可判定:
①m、p、q三点化学平衡常数Km、Kp、Kq的大小关系为Km>Kp=Kq.
②实际生产条件控制250℃,1.3×lO4Pa左右,选择此压强的理由是在250℃,1.3×lO4Pa时,CO转化率已较高,再增大压强,CO转化率提高不大,而生产成本增加,得不偿失.
 通过化学加工使煤转化为气体、液体、固体燃料,工业上用CO和H2合成CH3OH,请回答下列问题.
通过化学加工使煤转化为气体、液体、固体燃料,工业上用CO和H2合成CH3OH,请回答下列问题.(1)恒容密闭容器中,将水蒸气通过红热的炭,产生水煤气.反应为C(s)+H2O(g)?CO(g)+H2(g),除升高温度、使用催化剂外,能够使该反应速率增大的措施有增大H2O(g)的浓度.
(2)将不同量的CO(g)和H2O(g)分别通入到容积为2L的恒容密闭容器中,进行下列反应CO(g)+H2O(g)?CO2(g)+H2(g),得到数据如下:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO(g) | H2 | CO(g) | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 1.5 | 2 |
| 3 | 2 | 4 | 1.0 | n | t | |
②实验2中,v(CO2)=0.125mol•L-1•min-1,n=3;
③实验2和实验3中CO的转化率关系为:前者等于后者(填“大于”、“等于”、“小于”).
(3)工业上用CO(g)+2H2(g)?CH3OH(g)合成(CH3OH)具有重要意义.把一定物质的量的反应物投料于一恒容容器中,测得不同温度下CO转化率与温度和压强的关系,根据如图可判定:
①m、p、q三点化学平衡常数Km、Kp、Kq的大小关系为Km>Kp=Kq.
②实际生产条件控制250℃,1.3×lO4Pa左右,选择此压强的理由是在250℃,1.3×lO4Pa时,CO转化率已较高,再增大压强,CO转化率提高不大,而生产成本增加,得不偿失.
7.以下转化不能通过一步反应实现的是( )
| A. | Al2O2→Al(OH)3 | B. | Al→NaAlO2 | C. | Fe→FeCl2 | D. | Na→NaOH |
 某化学小组设计了铜与浓、稀硝酸反应的一体化实验装置如图所示(部分固定装置省略),实验步骤如下.请回答下列问题:
某化学小组设计了铜与浓、稀硝酸反应的一体化实验装置如图所示(部分固定装置省略),实验步骤如下.请回答下列问题: