题目内容
9.下列说法不正确的是( )| A. | 甘油作护肤保湿剂是因为甘油有还原性 | |
| B. | 服用铬含量超标的药用胶囊会对人对健康造成危害 | |
| C. | “血液透析”利用了胶体的性质 | |
| D. | 葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
分析 A、含有羟基数目较多的多羟基醇具有吸水性;
B、药用胶囊超标的铬,是重金属盐,能使蛋白质发生变性;
C、血液为胶体,“血液透析”运用了胶体的性质;
D、苏打是碳酸钠,依据葡萄中的花青素在碱性环境下显蓝色信息进行解答.
解答 解:A、甘油是含有羟基数目较多的多羟基醇,具有吸水性而作护肤保湿剂,故A错误;
B.铬是重金属,能使蛋白质发生变性,服用铬含量超标的药用胶囊会对人体健康造成危害,故B正确;
C.利用血液透析进行治疗因肾功能衰竭等疾病引起的血液中毒,是利用来了血液是胶体,不会通过半透膜的原理,故C正确;
D、苏打是碳酸钠,碳酸钠水解,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-溶液呈碱性,依据葡萄中的花青素在碱性环境下显蓝色信息可知,如果是假红酒,就没有葡萄糖,就不显蓝色,所以可用苏打粉检验假红酒,故D正确;
故选A.
点评 本题考查了胶体、甘油、重金属等物质的基本性质的应用,难度不大,注意知识的归纳和梳理是关键.

练习册系列答案
相关题目
17.对Na、Mg、Al的有关性质的叙述正确的是( )
| A. | 碱性:NaOH<Mg(OH)2<Al(OH)3 | B. | 价电子数:Na<Mg<Al | ||
| C. | 电负性:Na>Mg>Al | D. | 第一电离能:Na<Mg<Al |
4.某羧酸酯的分子式为C19H28O5,1mol该酯完全水解可得到羧酸的分子式为( )
| A. | C15H22O5 | B. | C15H20O5 | C. | C15H18O5 | D. | C15H24O5 |
14.常温下,电解质溶液中的下列关系式不正确的是( )
| A. | 已知A-+H2B(过量)═HA+HB-,则结合H+的能力:HB-<A-<B2- | |
| B. | 在0.1 mol?L-1的氨水中滴加0.1 mol?L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=10-a mol?L-1 | |
| C. | 将c mol?L-1的醋酸溶液与0.02 mol?L-1NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=$\frac{{2×1{0^{-9}}}}{c-0.02}$ | |
| D. | 将0.2 mol•L-1盐酸与0.1 mol•L-1的KAlO2溶液等体积混合,溶液中离子浓度由大到小的顺序: c(Cl-)>c(K+)>c(Al3+)>c(H+)>c(OH-) |
1.阿司匹林(主要成分为乙酰水杨酸)是解热止痛、治疗感冒的药物.它是由水杨酸(邻羟基苯甲酸)与醋酸酐进行酯化反应制得的.其反应原理如下:
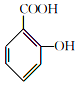 +
+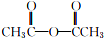 $→_{75-80℃}^{H_{3}PO_{4}}$
$→_{75-80℃}^{H_{3}PO_{4}}$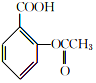 +CH3COOH
+CH3COOH
为避免醋酸酐水解,所用原料、仪器要充分干燥.有关物质的参数如表:
制取阿司匹林的工艺流程如下:
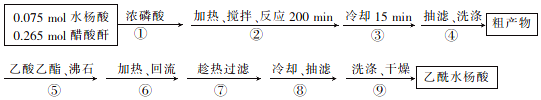
回答下列问题:
(1)浓磷酸的作用是催化剂.步骤②的加热方式为水浴加热,温度控制在75~80℃.
(2)向粗产物中加入乙酸乙酯的作用是溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失.
(3)验证最后得到的乙酰水杨酸产品较为纯净的方法是测定产品熔点.
(4)精制后乙酰水杨酸的质量为8.91g,则其产率为66%,造成产率低的原因可能有反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等)(任写一点).
 +
+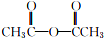 $→_{75-80℃}^{H_{3}PO_{4}}$
$→_{75-80℃}^{H_{3}PO_{4}}$ +CH3COOH
+CH3COOH为避免醋酸酐水解,所用原料、仪器要充分干燥.有关物质的参数如表:
| 名称 | 式量 | 性质 | 熔点/℃ | 沸点/℃ | 溶解度 | ||
| 水 | 乙醇 | 乙酸乙酯 | |||||
| 水杨酸 | 138 | 白色结晶粉末、无臭 | 157~159 | 211 | 溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 无色液体、易燃、有醋酸味 | -73.1 | 138.6 | 易溶 | 溶 | 易溶 |
| 乙酸水杨酸 | 180 | 白色针状结晶 | 135 | 321.4 | 冰水微溶、热水可溶 | 易溶 | 微溶 |

回答下列问题:
(1)浓磷酸的作用是催化剂.步骤②的加热方式为水浴加热,温度控制在75~80℃.
(2)向粗产物中加入乙酸乙酯的作用是溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失.
(3)验证最后得到的乙酰水杨酸产品较为纯净的方法是测定产品熔点.
(4)精制后乙酰水杨酸的质量为8.91g,则其产率为66%,造成产率低的原因可能有反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等)(任写一点).
18.下列A、B、C、D四个同学的陈述完全正确的是( )
| A. | NaCl:我是离子化合物,含有极性键 | |
| B. | H2O:我1mol中含有2mol非极性键 | |
| C. | KOH:既含有离子键,又含有极性共价键 | |
| D. | NaNO3:我是含有离子键的共价化合物 |
11.一种气态烷烃和一种气态烯烃组成的混合物共11.6g,混合气体的密度是相同状况下H2密度的14.5倍,该混合气体通过Br2水时,Br2水的质量增加8.4g,则组成该混合气体的可能是( )
| A. | 甲烷、乙烯 | B. | 乙烷、乙烯 | C. | 乙烷、丙烯 | D. | 甲烷、丙烯 |
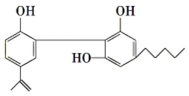 运动员服用兴奋剂的现象在世界大赛中时有发生,某种兴奋剂的结构如图.
运动员服用兴奋剂的现象在世界大赛中时有发生,某种兴奋剂的结构如图.